
科目: 来源: 题型:选择题
| A. | 原子半径C>A>B>D | B. | 价电子数D>C>A>B | ||
| C. | 离子半径C3+>D->B+>A2+ | D. | 单质的还原性A>B>C>D |
查看答案和解析>>
科目: 来源: 题型:解答题

 +NaHCO3→
+NaHCO3→ +H2O+CO2↑;
+H2O+CO2↑;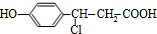 +3NaOH$→_{△}^{水}$
+3NaOH$→_{△}^{水}$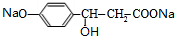 +NaCl+2H2O.
+NaCl+2H2O.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
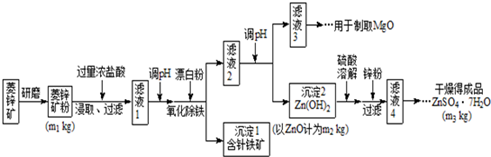
| Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 | |
| 开始沉淀的pH | 10.4 | 6.4 | - | - |
| 沉淀完全的pH | 12.4 | 8.0 | - | - |
| 开始溶解的pH | - | 10.5 | - | - |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
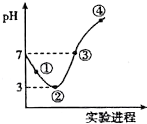 常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )
常温下,将Cl2缓慢通入100mL水中至饱和,然后向所得饱和氯水中逐滴加入0.1mol/L NaOH溶液,整个过程中pH的变化如图所示.下列有关叙述正确的是( )| A. | 用pH试纸测①处c(H+)约为②处c (H+)的两倍 | |
| B. | 可依据②处数据计算所溶解的n(Cl2) | |
| C. | ③处表示溶液中,c(Na+)=c(ClO-)+c(Cl-) | |
| D. | 曲线③④段有离子反应:HClO+OH-→ClO-+H2O |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 向稀盐酸中加入少量钠粒:2Na+2H2O→2Na++2OH-?+H2↑ | |
| B. | NaHSO4溶液与Ba(OH)2溶液混合呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| C. | 用漂白粉溶液吸收尾气中SO2:Ca2++2ClO-+SO2+H2O→CaSO3↓+2HClO | |
| D. | 向含氯化铝的氯化镁溶液中加入氧化镁:2Al3++3MgO+3H2O=2Al(OH)3↓+3Mg2+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4L的NO2和CO2混合气体中含有的氧原子数为4NA | |
| B. | 密闭容器中,46gNO2和N2O4的混合气体所含分子个数为NA | |
| C. | 常温常压下,22.4L的液态水含有2.24×10-8NA个OH- | |
| D. | 高温下,16.8 g Fe与足量水蒸气完全反应失去0.8NA个电子 |
查看答案和解析>>
科目: 来源: 题型:多选题
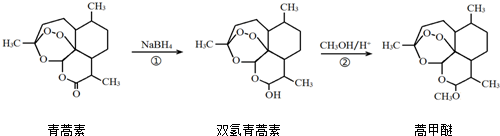
| A. | 青蒿素的分子式是C15H21O4 | |
| B. | 青蒿素在NaOH溶液中可以发生水解反应 | |
| C. | 反应②有H2O生成 | |
| D. | 反应①氧化反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D |
 |  |  | 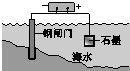 |
| 钢铁表面水膜的酸性很弱或呈中性,发生吸氧腐蚀 | 钢铁表面水膜的酸 性较强,发生析氢 腐蚀 | 将锌板换成铜板对 钢闸门保护效果更好 | 钢闸门作为阴极而受到保护 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com