
科目: 来源: 题型:选择题
| A. | 氯气通入水中 Cl2+H2O?H++Cl-+HClO | |
| B. | 甲烷的完全燃烧CH4(g)+2O2(g)$\frac{\underline{\;点燃\;}}{\;}$ CO2(g)+2H2O(l)△H<0 | |
| C. | 冰醋酸加入水中CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 铁与水蒸气反应 2Fe+3H2O$\frac{\underline{\;高温\;}}{\;}$ Fe2O3+3H2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 某品牌化妆品声称“我们拒绝化学,本品不含任何化学物质” | |
| B. | 用漂粉精和洁厕灵的混合液清洗马桶效果更佳 | |
| C. | 最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物 | |
| D. | 新核素的发现意味着新元素的合成 |
查看答案和解析>>
科目: 来源: 题型:选择题
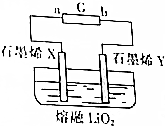 据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )
据英国《金融时报》网站最近报道,英国科学家研制出一种超容量的锂电池.其简易电池工作原理如图所示.X、Y是用石墨烯制成的渗透性极好的“蓬松”电极,其中石墨烯X极附着锂.该电池的工作原理是Li(s)+O2(g)$?_{充电}^{放电}$LiO2(s).下列说法不正确的是( )| A. | 充电过程,电源G的b极为负极 | |
| B. | 放电过程,Y极发生还原反应 | |
| C. | 放电过程,X极的电极反应式为Li-e-+O2-═LiO2 | |
| D. | 充电过程,每转移2 mol电子,Y极放出44.8L(标准状况)O2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙烯使溴水褪色;乙醇使高锰酸钾溶液褪色 | |
| B. | 油脂的皂化反应;乙烯制乙醇 | |
| C. | 蔗糖水解;乙醇和乙酸制乙酸乙酯 | |
| D. | 苯制溴苯;苯和氢气制环己烷 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCO3-的水解程度大于电离程度 | B. | HCO3-的水解程度小于电离程度 | ||
| C. | HCO3-的水解程度等于电离程度 | D. | 不能确定 |
查看答案和解析>>
科目: 来源: 题型:解答题
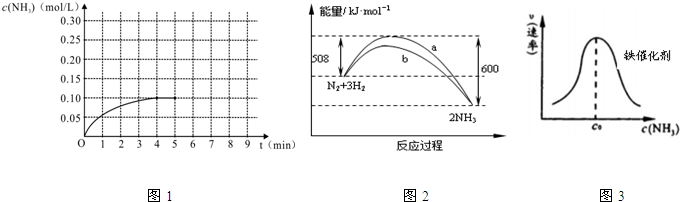
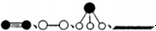 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示:
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用下图表示: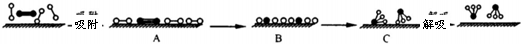
查看答案和解析>>
科目: 来源: 题型:解答题
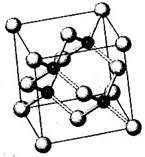 N、P、As、Ga、Cr等元素化合物种类繁多,具有重要的研究价值和应用价值.请回答下列问题:
N、P、As、Ga、Cr等元素化合物种类繁多,具有重要的研究价值和应用价值.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
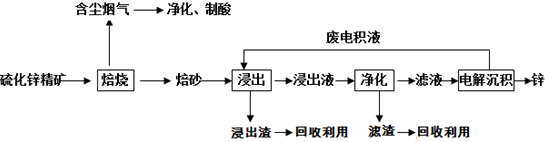
查看答案和解析>>
科目: 来源: 题型:解答题
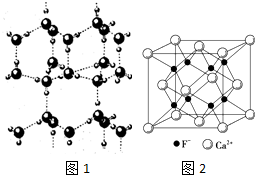 (1)下列分子中,属于平面型构型的有CD.
(1)下列分子中,属于平面型构型的有CD.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com