
科目: 来源: 题型:解答题
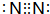 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 阴极增重1.72g | B. | 所得溶液 pH<1 | C. | 阴极增重0.64g | D. | 所得溶液pH>1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,将铁片置于浓硝酸中:Fe+6HNO3═Fe(NO3)3+3NO2↑+3H2O | |
| B. | Fe3O4与稀硝酸反应:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向硝酸亚铁溶液中加入稀盐酸:3Fe2++2H++$NO_3^-$═3Fe3++NO↑+H2O | |
| D. | 向浓硝酸中加入铜片:Cu+4H++2$NO_3^-$═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 汽油中绝不含铅元素 | B. | 汽油中不人为添加含铅元素的物质 | ||
| C. | 汽油中含铅元素在一定指标范围内 | D. | 以上都不正确 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 22.4L | B. | 11.2L | C. | 44.8L | D. | 89.6L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com