
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al、Cu、Mg、Ag、Fe | B. | Fe、Cu、Al、Ag、Mg | C. | Mg、Ag、Al、Cu、Fe | D. | Mg、Cu、Al、Ag、Fe |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 8n | B. | 18n | C. | 13n | D. | 44n |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 28g乙烯所含共用电子对数目为4NA | |
| B. | 1mol C4H10分子中共价键总数为13NA | |
| C. | 1 mol甲基所含的电子总数为7NA | |
| D. | 标准状况下,11.2 L己烷所含分子数为0.5 NA |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
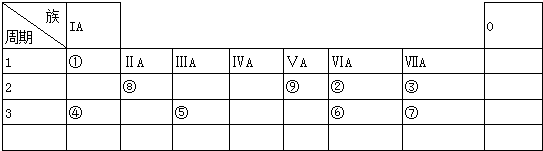
 ):
):
 、F
、F .
. 、⑨
、⑨ .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加入盐酸,产生白色沉淀,则试样中一定有Ag+ | |
| B. | 加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32-或HCO3- | |
| C. | 加入NaOH溶液微热,产生使湿润红色石蕊试纸变蓝气体,则试样中一定有NH4+ | |
| D. | 加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,则试样中一定有SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com