
科目: 来源: 题型:解答题

 (R、R′代表烃基)
(R、R′代表烃基)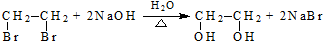 .
. .
. (C10H10O4)的同分异构体中,满足下列条件的有5种.
(C10H10O4)的同分异构体中,满足下列条件的有5种.查看答案和解析>>
科目: 来源: 题型:解答题
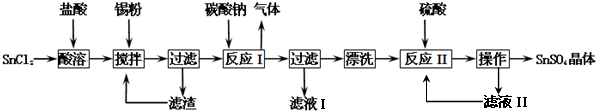
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加入NaOH溶液产生红褐色沉淀,则原溶液中一定有FeCl3 | |
| B. | 加入盐酸产生能使澄清石灰水变浑浊的气体,则原溶液中一定是CO32-或SO32- | |
| C. | 先通入少量Cl2后,再加入淀粉溶液后,溶液变蓝,说明有I- | |
| D. | 往溶液中加入BaCl2溶液和稀HNO3,有白色沉淀生成,说明一定有SO42- |
查看答案和解析>>
科目: 来源: 题型:解答题

 、C
、C .反应④所用试剂和条件是氢氧化钠醇溶液、加热.
.反应④所用试剂和条件是氢氧化钠醇溶液、加热. .
.查看答案和解析>>
科目: 来源: 题型:选择题
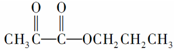 ,最简便的流程需要下列反应的顺序是
,最简便的流程需要下列反应的顺序是| A. | b d f g h | B. | e a d c h | C. | b a e c h | D. | e d c a h |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CH2═CH2 | B. | CH3CH═CH2 | C. | CH3CH2CH═CH2 | D. | CH3CH2CH2CH═CH2 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 时间(s) | 0 | 10 | 20 | 25 | 30 |
| 条件A[n(NO2)](mol) | 0.20 | 0.14 | 0.13 | 0.13 | 0.13 |
| 条件B[n(NO2)](mol) | 0.20 | 0.10 | 0.10 | 0.10 | 0.10 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na、Mg、Al最外层电子数依次增多,其还原性依次增强 | |
| B. | P、S、Cl最高正价依次升高,对应气态氢化物稳定性依次增强 | |
| C. | C、N、O原子半径依次增大 | |
| D. | Na和K属于第ⅠA族元素,其氧化物的水化物碱性:NaOH比KOH强 |
查看答案和解析>>
科目: 来源: 题型:解答题
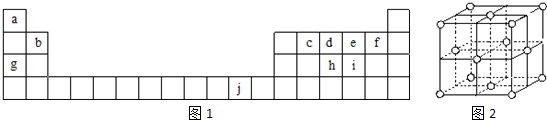
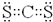 ,ci2与ce2比较,沸点较高的是CS2(写分子式).
,ci2与ce2比较,沸点较高的是CS2(写分子式).查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com