
科目: 来源: 题型:选择题
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 分离苯和乙酸的混合物 | 分液漏斗、烧杯 | |
| B | 鉴别葡萄糖和乙酸甲酯 | 试管、烧杯、酒精灯 | 葡萄糖溶液、乙酸甲酯溶液、银氨溶液 |
| C | 实验室制取CO2 | 试管、带导管的橡胶塞 | 大理石、稀硫酸 |
| D | 测定未知NaOH溶液浓度 | 酸、碱式滴定管、锥形瓶、烧杯 | NaOH溶液、0.1mol/L盐酸标准液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用氯胺处理自来水:NH2Cl+H2O?NH2OH+HCl | |
| B. | 在含有Mg2+、HCO3-的自来水中加入过量的澄清石灰水:Ca2++Mg2++2OH-+2HCO3-═CaCO3↓+MgCO3↓+2H2O | |
| C. | 长时间煮沸含Mg2+、HCO3-的自来水:Mg2++2HCO3-$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+2CO2↑ | |
| D. | Na2FeO4既是混凝剂、又可作消毒剂,作混凝剂的作用原理为:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
查看答案和解析>>
科目: 来源: 题型:解答题
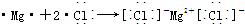 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
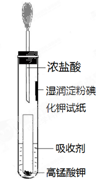 氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
氯气是氯碱工业的主要产品之一,它是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:查看答案和解析>>
科目: 来源: 题型:选择题
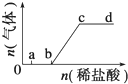 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )| A. | a点对应的溶液中:Na+、OH-、SO42-、NO3- | |
| B. | b点对应的溶液中:Al3+、Fe3+、SCN-、Cl- | |
| C. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应的溶液中:SO32-、Na+、Cl-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe与稀HNO3 | B. | Na2O2与CO2 | ||
| C. | NaOH溶液与CO2 | D. | AlCl3溶液与NaOH溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ag+、NO3-、Cl-、K+ | B. | Na+、Fe2+、Cl-、NO3- | ||
| C. | K+、Ba2+、OH-、SO42- | D. | Cu2+、NH4+、Br-、Cl- |
查看答案和解析>>
科目: 来源: 题型:解答题
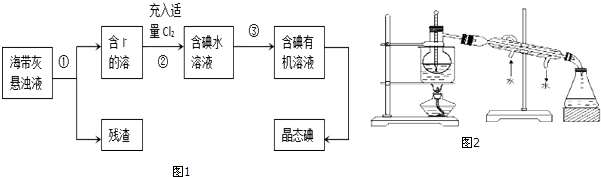
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com