
科目: 来源: 题型:选择题
| A. | 将饱和氯化铁溶液滴入氢氧化钠溶液中即可 | |
| B. | 将饱和氯化铁溶液滴入热水中,生成棕黄色液体即可 | |
| C. | 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色液体即可 | |
| D. | 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 化合物与纯净物属于重叠关系 | |
| B. | 化合物与氧化物属于交叉关系 | |
| C. | 分解反应与复分解反应属于并列关系 | |
| D. | 钠盐与碳酸盐属于并列关系 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将纯水加热到950C时,Kw变大,pH不变,水仍呈中性 | |
| B. | 向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 | |
| C. | 向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,KW不变 | |
| D. | 向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCO3-、Ag+、NO3-、Na+ | B. | Na+、Cl-、CO32-、NO3- | ||
| C. | Fe3+、Na+、Cl-、SO42- | D. | H+、Cl-、CO32-、NH4+ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 编号 | 操作 | 现象 |
| Ⅰ | 向2 mL 0.1 mol/LFeCl2溶液中滴加KSCN溶液,再滴加氯水 | |
| Ⅱ | 向2 mL 0.1 mol/L FeCl3溶液中滴加KSCN溶液,再滴加0.1 mol/L KI溶液 | 滴加KSCN溶液后,溶液变成红色; 滴加KI溶液后,红色无明显变化 |
| 编号 | 操作 | 现象 |
| Ⅲ | 向2 mL 0.1 mol/L KI溶液中滴加1 mL 0.1 mol/L FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色; 滴加KSCN溶液后,溶液变成红色 |
| 编号 | 操作 | 预期现象及结论 |
| Ⅳ | 向2 mL 0.1 mol/L KI溶液中滴加 1 mL 0.1mol/L FeCl3溶液,或CCl4;或铁氰化钾溶液 | 溶液变蓝(或溶液分层,下层溶液为紫色;或生成蓝色沉淀),结论:Fe3+能与I-发生氧化还原反应,生成I2(或Fe2+) |
查看答案和解析>>
科目: 来源: 题型:解答题
 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应:查看答案和解析>>
科目: 来源: 题型:解答题
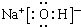 .
.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com