
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K=$\frac{[C]•[{H}_{2}O]}{[CO]•[{H}_{2}]}$ | B. | K=$\frac{[CO]•[{H}_{2}]}{[C]•[{H}_{2}O]}$ | C. | K=$\frac{[CO]•[{H}_{2}]}{[{H}_{2}O]}$ | D. | K=$\frac{[{H}_{2}O]}{[CO]•[{H}_{2}]}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 3:2:3 | B. | 3:1:2 | C. | 2:6:3 | D. | 1:1:1 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
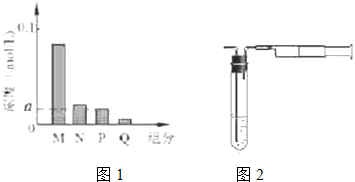 已知X、Y是两种性质相似的短周期元素.
已知X、Y是两种性质相似的短周期元素.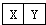 ,它们的单质都必须采用电解法制备,但都无需密封保存,
,它们的单质都必须采用电解法制备,但都无需密封保存,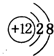 .(2)Y元素在周期表中位置第三周期ⅢA族.
.(2)Y元素在周期表中位置第三周期ⅢA族.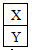 ,X是形成化合物种类最多的元素.
,X是形成化合物种类最多的元素. ,X、Y的最高价含氧酸的浓溶液都有强氧化性.
,X、Y的最高价含氧酸的浓溶液都有强氧化性.查看答案和解析>>
科目: 来源: 题型:选择题
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 氢化物的沸点排序:Y>T>R | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 单质氧化性:Y>R>T |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2 | B. | MgCl2 | C. | BF3 | D. | PCl3 |
查看答案和解析>>
科目: 来源: 题型:解答题
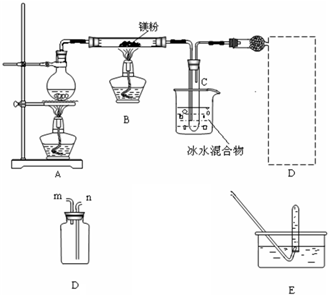
查看答案和解析>>
科目: 来源: 题型:多选题
| 选项 | 陈述I | 陈述II |
| A | 酸性:HCl>H2CO3 | 非金属性:Cl>C |
| B | K+、Ca2+、Mg2+ 的离子半径依次减小 | K+、Ca2+、Mg2+氧化性性依次增强 |
| C | 硬铝是合金 | 其熔点比金属铝的熔点低 |
| D | 电镀时阳极上发生还原反应 | 可在铁的镀件上镀铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com