
科目: 来源: 题型:
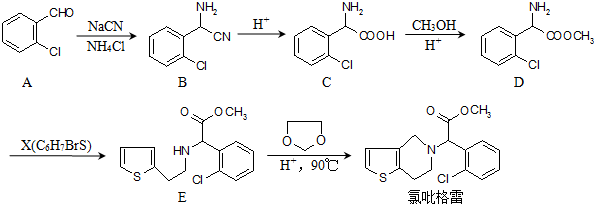


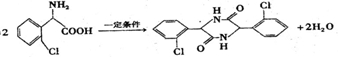

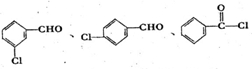

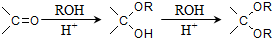
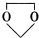 的合成路线流程图(无机试剂任选).合成路线流程示意图为:
的合成路线流程图(无机试剂任选).合成路线流程示意图为: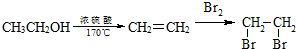
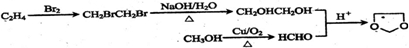
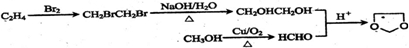
查看答案和解析>>
科目: 来源: 题型:阅读理解

| ||
查看答案和解析>>
科目: 来源: 题型:
| 3 |
| 4 |


| ||
| ||
查看答案和解析>>
科目: 来源: 题型:
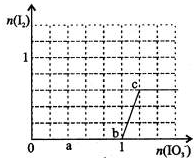 已知:还原性HSO-3>I-,氧化性IO-3>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如右图所示.下列有关说法正确的是( )
已知:还原性HSO-3>I-,氧化性IO-3>I2.在含3mol NaHSO3的溶液中逐滴加入KIO3溶液.加入KIO3和析出I2的物质的量的关系曲线如右图所示.下列有关说法正确的是( )查看答案和解析>>
科目: 来源: 题型:
 已知可逆反应:FeO(s)+CO(g)
已知可逆反应:FeO(s)+CO(g) Fe(s)+CO2(g)是炼铁工业中的一个重要反应,其温度T与n(CO2)/n(CO)的比值关系如右下表所示.下列有关说法正确的是( )
Fe(s)+CO2(g)是炼铁工业中的一个重要反应,其温度T与n(CO2)/n(CO)的比值关系如右下表所示.下列有关说法正确的是( )查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com