
科目: 来源: 题型:选择题
| A. | 晶体硅是良好的半导体材料 | |
| B. | 硅单质可用来制造太阳能电池 | |
| C. | SiO2是制造光导纤维的材料 | |
| D. | 可用带玻璃塞的试剂瓶中盛有NaOH溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 稀醋酸与氢氧化钠溶液反应:H++OH-═H2O | |
| B. | 铜粉与稀硝酸反应:Cu+2H+═Cu2++H2↑ | |
| C. | 氯气与碘化钾溶液反应:Cl2+2I-═I2+2Cl- | |
| D. | 碳酸钙与足量盐酸反应:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 高锰酸钾中含有氧元素,属于氧化物 | |
| B. | 一氧化碳中含有碳元素,属于有机物 | |
| C. | 纯碱溶液显碱性,属于碱 | |
| D. | 绿矾的化学式为FeSO4•7H2O,属于纯净物 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入粉末质量/g | 13.68 | 27.36 | 34.20 |
| 生成气体的体积(标准状况)/L | 2.912 | 5.824 | 6.720 |
查看答案和解析>>
科目: 来源: 题型:解答题
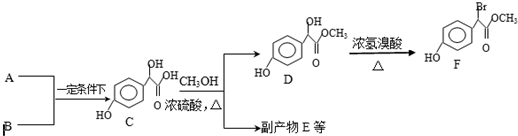
 .
.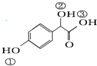 )中①、②、③3个-OH的酸性由强到弱的顺序是:③>①>②.
)中①、②、③3个-OH的酸性由强到弱的顺序是:③>①>②. 任意2种.
任意2种.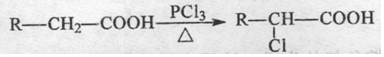 A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选).合成路线流程图示例如下:
A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选).合成路线流程图示例如下:查看答案和解析>>
科目: 来源: 题型:解答题
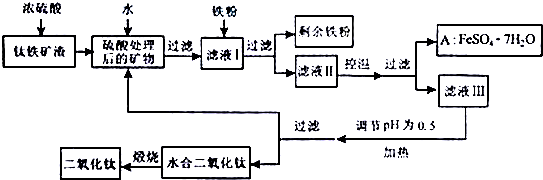
查看答案和解析>>
科目: 来源: 题型:解答题
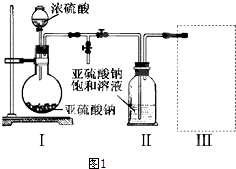
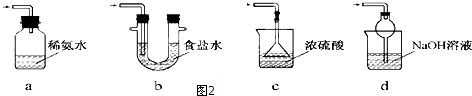

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com