
科目: 来源: 题型:选择题
| A. | NaOH可用于治疗胃酸过多 | |
| B. | CaO可防止月饼等食品氧化变质 | |
| C. | 氢弹中用到的2H、3H互为同位素 | |
| D. | 向海水中加入净水剂明矾可以使海水淡化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D |
带玻璃塞的试剂瓶 | 聚乙烯盒 | 铁罐车 | 铝制饭盒 |
| 可用于盛放氢氧化钠溶液 | 可用于盛装食品 | 可用于运输浓硫酸 | 不宜长时间存放酸性或碱性的食物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
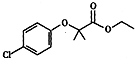
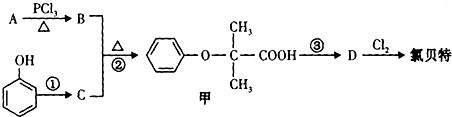
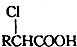

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:多选题
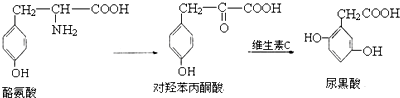
| A. | 1mol酪氨酸能与含1molHCl的盐酸反应,又能与含2molNaOH的溶液反应 | |
| B. | 酪氨酸能发生加成、取代、消去和缩聚反应 | |
| C. | 1mol对羟苯丙酮酸最多可与5molH2反应 | |
| D. | 1mol尿黑酸最多可与3molBr2反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向Ca(HCO3)2溶液中加入足量的NaOH溶液:Ca2++HCO3-+OH-→CaCO3↓+H2O | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO42ˉ恰好完全反应:2Ba2++4OH-+Al3++2SO42-→BaSO4↓+AlO2-+2H2O | |
| C. | 足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O→2HCO3- | |
| D. | 向Fe2(SO4)3溶液中加入过量Na2S溶液:2Fe3++3S2-→2FeS↓+S↓ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①④ | B. | ①② | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
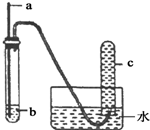 用下图所示装置进行实验,实验现象对应的结论正确的是( )
用下图所示装置进行实验,实验现象对应的结论正确的是( )| a | b | 实验现象 | 结论 | |
| A | 铜丝 | 稀硝酸 | c中收集到大量无色气体 | 稀硝酸与铜反应生成NO2 |
| B | 木条 | 18.4mol/L浓硫酸 | 木条变黑 | 浓硫酸具有酸性 |
| C | 铁钉 | 饱和食盐水 | 部分水进入导管 | 铁钉发生吸氧腐蚀 |
| D | 铝片 | 浓硝酸 | 无明显现象 | 铝与浓硝酸不反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶液中c(OH-)减小 | B. | pH的变化值等于2 | ||
| C. | 溶液中H+的个数增大 | D. | Kw的值减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com