
科目: 来源: 题型:解答题
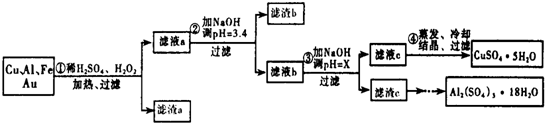
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 3.2 | 5.2 | 6.7 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 若某钠盐溶液含甲电离出的阴离子,则该溶液既可能与酸反应又可能与碱反应 | |
| B. | 若乙与氧气的摩尔质量相同,则乙只能由2种元素组成 | |
| C. | 若丙中含有第2周期ⅣA族的元素,则丙可能是甲烷的同系物 | |
| D. | 若丁中各元素质量比跟甲中各元素质量比相同,则丁中一定含有-1价的元素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++H++OH-+SO42-═BaSO4↓+H2O | |
| B. | NH4HCO3溶液与少量KOH浓溶液共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 向浓硝酸中加入铜片,Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 二氧化硫通入次氯酸钙溶液:SO2+Ca2++2ClO-+H2O═CaSO3↓+2HClO |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源:2016-2017学年天津市高一上9月调研化学试卷(解析版) 题型:选择题
仅依据下表给出的物理量X和Y,其中不能求出物质的量的是
A | B | C | D | |
X | 物质中的粒子数 | 标准状况下的 气体摩尔体积 | 固体的体积 | 溶液中溶质的 物质的量浓度 |
Y | 阿伏加德罗常数 | 标准状况下 气体的体积 | 固体的密度 | 溶液体积 |
查看答案和解析>>
科目: 来源: 题型:多选题
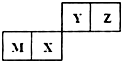
| A. | M与Z形成的化合物中只存在离子键 | |
| B. | X的最简单气态氢化物的热稳定性比Z的强 | |
| C. | 原子半径Z>Y | |
| D. | M的最高价氧化物对应水化物能与NaOH溶液反应 |
查看答案和解析>>
科目: 来源: 题型:填空题
 如图为某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液中S2-浓度,金属阳离子浓度变化情况.如果向含有这三种沉淀的混合物中加盐酸,最先溶解的是FeS.
如图为某温度下,CuS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液中S2-浓度,金属阳离子浓度变化情况.如果向含有这三种沉淀的混合物中加盐酸,最先溶解的是FeS.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com