
科目: 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 氢气可以在氯气中燃烧,说明燃烧反应未必需要氧气参与 | |
| C. | 足量Cl2、S分别和二份等质量的Na反应,两者得到电子一样多 | |
| D. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸根本就不会反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | K+、Na+、CO32-、Cl- | B. | Ca2+、K+、CO32-、OH- | ||
| C. | Fe3+、Ba2+、NO3-、SO42- | D. | H+、Na+、Cu2+、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) | 溶解性 |
| 甲 | -68 | 115 | 0.93 | 易溶于水 |
| 乙 | -84 | 77 | 0.90 | 易溶于甲 |
| A. | 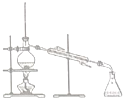 | B. | 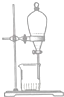 | C. | 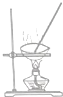 | D. | 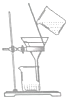 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2CO3和K2O都属于盐 | B. | H2SO4和HNO3都属于酸 | ||
| C. | KOH和Na2CO3都属于碱 | D. | Na2O和Na2SiO3都属于氧化物 |
查看答案和解析>>
科目: 来源: 题型:解答题
 实验小组的同学探究铁与浓、稀硝酸反应的还原产物.他们通过查资料得知:Nessler试剂(K2HgI4的KOH溶液)可与NH4+反应生成沉淀
实验小组的同学探究铁与浓、稀硝酸反应的还原产物.他们通过查资料得知:Nessler试剂(K2HgI4的KOH溶液)可与NH4+反应生成沉淀查看答案和解析>>
科目: 来源: 题型:解答题
 NH3•H2O+H+.
NH3•H2O+H+.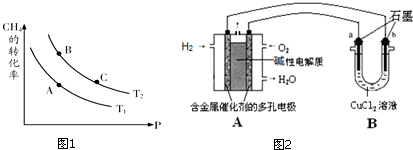
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 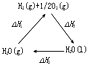 图中△H1=△H2+△H3 | |
| B. | 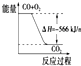 从图可看出CO2的能量高于CO+O2 | |
| C. |  从图可看出反应中加入催化剂可降低反应物能量 | |
| D. | 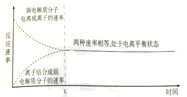 图中t0时间段后(不包含t0)电解质溶液中,弱电解质分子与离子都存在 |
查看答案和解析>>
科目: 来源: 题型:选择题
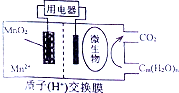
| A. | MnO2极为负极 | |
| B. | Cn(H2O)m发生了氧化反应 | |
| C. | 电子从负极区经交换膜移向正极区 | |
| D. | 放电过程中,H+从正极区移向负极区 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 最高价氧化物的水化物的碱性:Z>Y | B. | 离子的还原性:M>X | ||
| C. | 电子层数:Y<M | D. | 离子半径:Y<Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com