
科目: 来源: 题型:选择题
| A. | 从海水中提取溴、碘都涉及置换反应,从矿物质中获取铝、铁、铜、硅都不涉及置换反应 | |
| B. | 利用溶解度数据可推测将一些混合物质分离开来的可能性,利用原子半径数据可推测某些原子的氧化性和还原性的强弱 | |
| C. | 因为食盐能使细菌变性,所以可以用食盐水杀死H7N9禽流感病毒 | |
| D. | 某反应的△H>0、△S<0,则该反应一定不能正向进行 |
查看答案和解析>>
科目: 来源: 题型:解答题
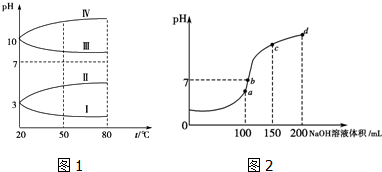
查看答案和解析>>
科目: 来源: 题型:解答题
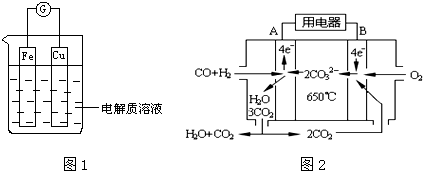
查看答案和解析>>
科目: 来源: 题型:选择题
| 组号 | 反应温度(℃) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O的体积(mL) | ||||
| 体积(mL) | 浓度(mol•L-1) | 体积(mL) | 浓度(mol•L-1) | |||
| A | 10 | 5.0 | 0.10 | 10.0 | 0.10 | 5.0 |
| B | 10 | 5.0 | 0.10 | 5.0 | 0.10 | 10.0 |
| C | 30 | 5.0 | 0.10 | 5.0 | 0.10 | 10.0 |
| D | 30 | 5.0 | 0.20 | 5.0 | 0.10 | 10.0 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 | |
| B. | 废旧电池不能随意丢弃,要进行深埋处理,防止重金属污染 | |
| C. | “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 | |
| D. | 人类日常利用的煤、天然气、石油等的能量,归根到底是由太阳能转变来的 |
查看答案和解析>>
科目: 来源: 题型:解答题
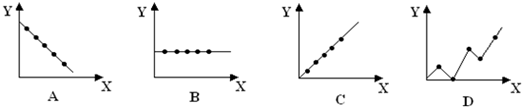
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
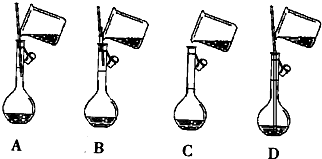
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com