
科目: 来源: 题型:解答题
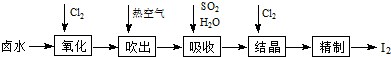
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 世博会期间,处理废水时加入明矾可作为混凝剂以吸附水中的悬浮物杂质且有杀菌消毒的作用 | |
| B. | 世博会期间,利用可降解的“玉米塑料”替代一次性饭盒,可防止产生白色污染 | |
| C. | 世博会中国馆--“东方之冠”使用了大量钢筋混凝土,混凝土是混合物 | |
| D. | 世博停车场安装光电设施,可将阳光转化为电能以供应照明 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe(NO3)2 | B. | Cu(NO3)2 | C. | Fe(NO3)3 | D. | HNO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①④⑥⑦ | B. | ④⑥⑧ | C. | ①②④⑤ | D. | ④⑥ |
查看答案和解析>>
科目: 来源: 题型:解答题
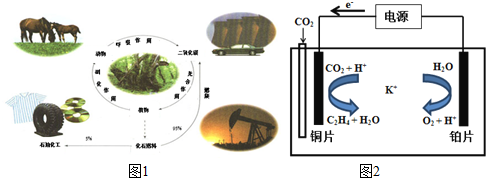
温度(℃) 气体总浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 9×10-3 | 2.7×10-2 | 8.1×10-2 |
| t2 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
| t3 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
查看答案和解析>>
科目: 来源: 题型:解答题
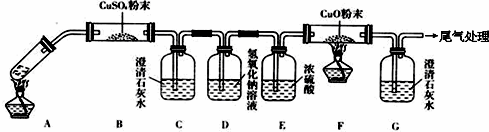
查看答案和解析>>
科目: 来源: 题型:解答题
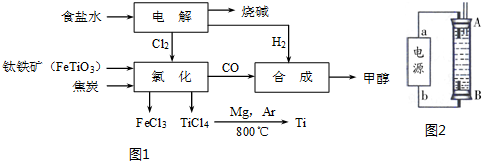
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
查看答案和解析>>
科目: 来源: 题型:解答题
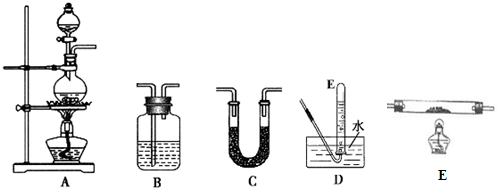
| 选用的仪器 | 加入的试剂 |
| A | 甲酸、浓硫酸 |
| D | -- |
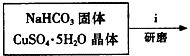
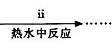
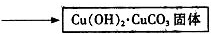
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 16O、18O互为同位素 | |
| B. | 金刚石和石墨互为同素异形体 | |
| C. | 分子式符合通式CnH2n+2且 n 值不同的两种烃互为同系物,而分子式符合通式CnH2n且 n 值不同的两种烃不一定互为同系物 | |
| D. | 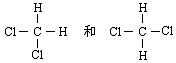 互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③ | B. | ①③⑤ | C. | ②④⑤ | D. | ③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com