
科目: 来源: 题型:选择题
| A. | 简单氢化物的热稳定性:Z>W | B. | 最高价氧化物的水化物的酸性:X<Z | ||
| C. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | D. | 沸点:XW2>Y2W |
查看答案和解析>>
科目: 来源: 题型:选择题
| 序号 | 实验内容 | 实验目的 |
| A | 常温下,测得饱和Na2CO3溶液的pH大于饱和 NaHCO3溶液的pH | 比较常温下水解程度: CO32->HCO3- |
| B | 向2mL甲苯中加入3滴KMnO4酸性溶液,振荡; 向2mL己烷中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶 液,前者为黄色,后者为红褐色 | 证明温度升高,Fe3+的水解程度 增大 |
| D | 向盛有10滴0.1mol/LAgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1mol/L Na2S溶液 | 证明AgCl沉淀能转化为溶解度更小 的Ag2S沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,11.2LCHCl3含有共价键数为2NA | |
| B. | 某温度下,纯水pH=6,该温度下1LpH=11的NaOH溶液中含有OH-数目为0.1NA | |
| C. | 含3.65gHCl的水溶液中含有粒子数为0.2NA | |
| D. | 0.2mol/LNa2S溶液中含有S2-数目小于0.2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺 | |
| B. | 四大发明之一黑火药是由硫黄、硝石、木炭三种物质按一定比例混合制成 | |
| C. | 工业上电解熔融状态的Al2O3制备Al | |
| D. | 为预防碘缺乏病,在食盐中加入碘单质 |
查看答案和解析>>
科目: 来源: 题型:解答题
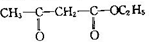 )和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示.
)和聚乙烯醇(PVA)都是重要的有机化工产品,其合成路线如图所示.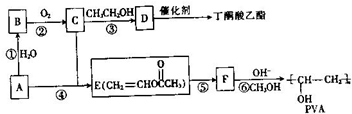
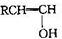 不稳定会自动转化为RCH2CHO.
不稳定会自动转化为RCH2CHO.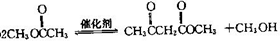
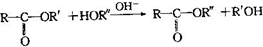
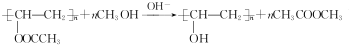 ,该反应的反应类型为取代反应.
,该反应的反应类型为取代反应.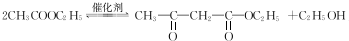 ,Na与生成的乙醇反应,平衡右移,提高D的转化率.(根据化学方程式和平衡移动原理回答)
,Na与生成的乙醇反应,平衡右移,提高D的转化率.(根据化学方程式和平衡移动原理回答) 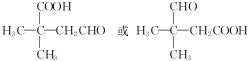 (填结构简式).
(填结构简式).查看答案和解析>>
科目: 来源: 题型:解答题
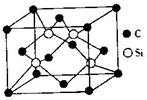 氮化硅是一种重要的结构陶瓷材料,具有优良性能.
氮化硅是一种重要的结构陶瓷材料,具有优良性能.查看答案和解析>>
科目: 来源: 题型:填空题
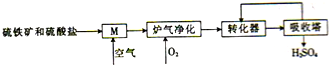 煤是重要的化工原料,煤的脱硫可减少环境的污染,利用煤矸石中的硫铁矿(主要成分为FeS2)和烟道脱硫得到的硫酸盐生产硫酸的工艺流程如图所示.
煤是重要的化工原料,煤的脱硫可减少环境的污染,利用煤矸石中的硫铁矿(主要成分为FeS2)和烟道脱硫得到的硫酸盐生产硫酸的工艺流程如图所示.查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 将浓硫酸入蔗糖中 | 固体变黑后发生膨胀 | 浓硫酸具有吸水性和强还原性 |
| B | 将两小粒相同的钠分别投入乙醇和水中 | 钠在水中反应比在乙醇中剧烈 | 相同条件下,水的电离能力比乙醇强 |
| C | 向某溶液滴加氯水后再滴入KCSN溶液 | 溶液变为红色 | 该溶液中一定含有Fe2+ |
| D | 常温时将铝片加入浓硝酸中 | 未出现气泡 | 常温下铝与浓硝酸不反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
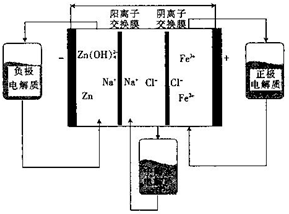
| A. | 放电时,Na+从中间室进入负极室 | |
| B. | 充电时,Cl-从阳极室进入中间室 | |
| C. | 放电时,负极的电极反应为Zn+4OH--2e-=Zn(OH)42- | |
| D. | 充电时,阳极的电极反应为Fe3++e-=Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com