
科目: 来源: 题型:选择题
| A. | 由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 | |
| B. | Ksp只与难溶电解质的性质和温度有关 | |
| C. | 其他条件不变,离子浓度改变时,Ksp不变 | |
| D. | 两种难溶电解质,Ksp小的,溶解度一定小 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
查看答案和解析>>
科目: 来源: 题型:解答题
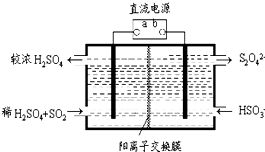 氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化.
氮和硫的氧化物有多种,其中SO2和NOx都是大气污染物,对它们的研究有助于空气的净化.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2.24 L CO2中含有的原子数为0.3×6.02×1023 | |
| B. | 0.1 mol F- 中含有的电子数等于0.9×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 电解饱和食盐水若产生2 g氢气,则转移的电子数目为2×6.02×1023 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 若m>n,金属性W>X | |
| B. | 若m>n,气态氢化物的稳定性HmY>HnZ | |
| C. | 若m<n,氧化性Xn+>Wm+ | |
| D. | 若m<n,原子序数a>b>c>d |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径:A>B>C>D | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D>C>B>A | D. | a+1=d-2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CaCl2和Na2CO3 | B. | 稀盐酸和Na[Al(OH)4] | C. | 稀盐酸和Na2CO3 | D. | NaOH和AlCl3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④ | B. | ③④⑤ | C. | ②③⑤ | D. | ①⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4种 | B. | 9种 | C. | 13种 | D. | 15种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ROH | B. | R2O7 | C. | HRO3 | D. | NaR |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com