
科目: 来源: 题型:解答题
 Na2O2具有强氧化性,可以用来漂白纺织类物品、麦杆、纤维等.
Na2O2具有强氧化性,可以用来漂白纺织类物品、麦杆、纤维等.查看答案和解析>>
科目: 来源: 题型:解答题
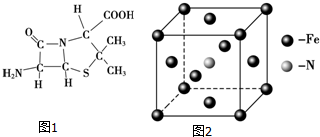
 )分子中有5n个σ键
)分子中有5n个σ键| 化学键 | Si-Si | O═O | Si-O |
| 键能(kJ•mol-1) | a | b | c |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

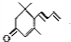 .(已知一个碳原子上不能连接两个碳碳双键)
.(已知一个碳原子上不能连接两个碳碳双键) +CH3COOH$→_{△}^{浓硫酸}$、
+CH3COOH$→_{△}^{浓硫酸}$、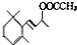 +H2O.
+H2O.
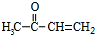 为原料制备聚1,3-丁二烯-{CH2-CH=CH-CH2}-n的合成路线.
为原料制备聚1,3-丁二烯-{CH2-CH=CH-CH2}-n的合成路线.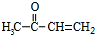 $\stackrel{NaBH_{4}}{→}$
$\stackrel{NaBH_{4}}{→}$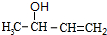 $→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{一定条件}{→}$
$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{一定条件}{→}$ .
.查看答案和解析>>
科目: 来源: 题型:选择题
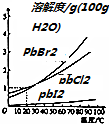
| A. | 三种卤化铅的溶解度均随温度的升高而减小 | |
| B. | 20℃时,PbCl2的Ksp约为1.87×10-4 | |
| C. | 任何温度下,始终存在:Ksp(PbCl2>Ksp(PbBr2>Ksp(PbI2) | |
| D. | 常温下,向浓度均为0.1mol•L-1的Cl-、Br-、I-混合溶液中,逐滴加入的Pb(NO3)2溶液,PbCl2最先沉淀 |
查看答案和解析>>
科目: 来源: 题型:解答题
 铁、钴、镍等金属及其化合物在工业上有重要用途.请回答:
铁、钴、镍等金属及其化合物在工业上有重要用途.请回答:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

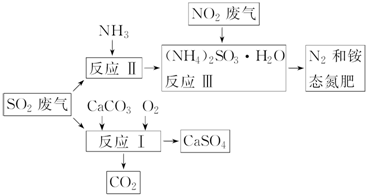

查看答案和解析>>
科目: 来源: 题型:选择题
| X | ||
| Y | Z |
| A. | 化合物XZ3中各原子均满足8电子的稳定结构 | |
| B. | X、Y、Z三种元素形成的含氧酸都是强酸 | |
| C. | 常温下,Z单质可与Y的氢化物发生置换反应 | |
| D. | Z的气态氢化物比Y的气态氢化物更加稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com