
科目: 来源: 题型:解答题
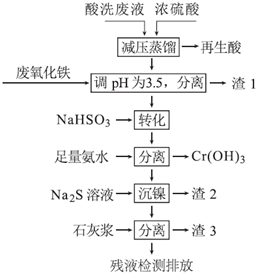
| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
查看答案和解析>>
科目: 来源: 题型:解答题
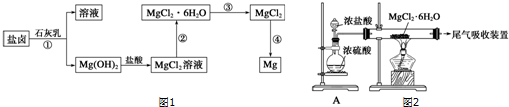
查看答案和解析>>
科目: 来源: 题型:解答题
 已知各种金属离子完全沉淀的pH如下表:
已知各种金属离子完全沉淀的pH如下表:| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2和氢气合成甲烷,实现“碳循环” | |
| B. | 提倡步行、骑自行车、乘公交车等“低碳”出行方式 | |
| C. | 采用纳米TiO2光触媒技术将装修材料中释放的HCHO转化为无害物质 | |
| D. | 将造纸废水通过高压水井压到地下或溶洞中,减少对地表水的污染 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{a}{A+m}$(Z+m)mol 质子 | B. | $\frac{a}{A}$(Z+m)mol 电子 | ||
| C. | $\frac{a}{A+m}$(A-Z+m)mol 中子 | D. | $\frac{a}{A}$mmolHmX |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 工业上常用MnO2和稀盐酸共热来制取氯气 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 在氧化还原反应中,Cl2只能作氧化剂 | |
| D. | 若含0.4 mol HCl的浓盐酸,MnO2过量,可制得标准状况下氯气2.24 L |
查看答案和解析>>
科目: 来源: 题型:解答题
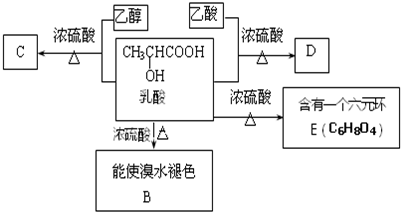
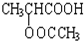 ;
;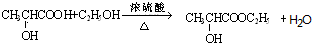 ;
;查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 液氨气化吸收大量热,可做制冷剂 | |
| B. | 晶体硅用于制作半导体材料是因其熔点高、硬度大 | |
| C. | 二氧化锰具有强氧化性,故能将双氧水氧化为氧气 | |
| D. | Fe比Cu活泼,所以FeCl3溶液可以腐蚀线路板上的Cu |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com