
科目: 来源: 题型:选择题
| A. | X与Y形成的两种化合物中阴、阳离子的个数比均为2:1 | |
| B. | Y的氢化物比R的氢化物稳定,Y的氢化物熔沸点比R的氢化物低 | |
| C. | Z、W、R最高价氧化物对应水化物的酸性强弱顺序:R>W>Z | |
| D. | Y分别与Z、W、R以两种元素组成的常见化合物有3种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向容量瓶或分液漏斗中注入溶液时,应该将两者口部的玻璃塞倒置在桌面上 | |
| B. | 在实验室做蒸馏实验的装置中用到两个铁架台、三个单孔胶塞 | |
| C. | 将等体积不同浓度的酸性高锰酸钾分别滴入等浓度体积的草酸溶液中,依据褪色快慢,比较浓度对翻译速率的影响 | |
| D. | 过量的浓硫酸与铜屑共热,能得到澄清透明的蓝色溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,2.24L Cl2通入足量水中或NaOH溶液中,转移的电子数均为0.1NA. | |
| B. | 1mol CnH2n含有的共用电子对数为(3n+1)NA | |
| C. | 电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子书为0.2NA | |
| D. | 2gD2160中含中子、质子、电子数目均为NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 新制氯水中存在两种电离平衡 | |
| B. | 不同原子之间形成的共价键不一定是极性共价键 | |
| C. | 向久置于空气中的Na2SiO3、NaOH、CaCl2、漂白粉溶液里加足量盐酸,都能产生气体 | |
| D. | 将少量酸化的FeCl2溶液滴入过氧化氢溶液中,溶液变黄,并产生大量的气泡. |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学可以识别、改变和创造分子 | |
| B. | 金刚石常用作砂纸、砂轮的磨料 | |
| C. | 氧化铁常用作红色油漆和涂料 | |
| D. | 葡萄糖可用于合成补钙药物及维生素C(结构如图)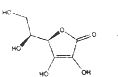 |
查看答案和解析>>
科目: 来源: 题型:解答题
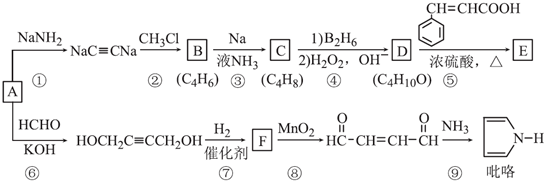
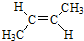 .
.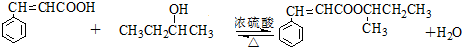 .
.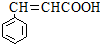 )的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有7种(不考虑顺反异构).与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是CH3CH2OCH2CH3.
)的同分异构体中,含有苯环和碳碳双键,且能够发生水解反应的共有7种(不考虑顺反异构).与D互为同分异构体,且核磁共振氢谱有面积比为2:3的两组峰的有机物的结构简式是CH3CH2OCH2CH3.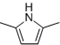 )的合成路线
)的合成路线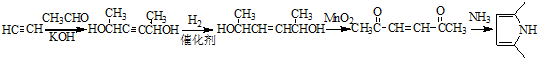 .
.查看答案和解析>>
科目: 来源: 题型:选择题
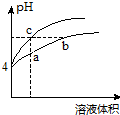 某温度下,体积和pH都相同的氯化铵溶液和盐酸加水稀释时的pH变化曲线如图所示.下列判断正确的是( )
某温度下,体积和pH都相同的氯化铵溶液和盐酸加水稀释时的pH变化曲线如图所示.下列判断正确的是( )| A. | a、c两点溶液的导电能力:c>a | |
| B. | a、b、c三点溶液中水的电离程度:a>b>c | |
| C. | b点溶液中:c(H+)=c(Cl-)+c(OH-) | |
| D. | 用NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液的体积Vb=Vc |
查看答案和解析>>
科目: 来源: 题型:解答题
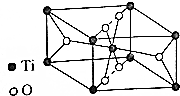 为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用.
为了实现“将全球温度上升控制在2℃以内”,科学家正在研究温室气体CH4和CO2的转化和利用. ,Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有σ键的数目为8NA.
,Ni能与CO形成正四面体形的配合物Ni(CO)4,1molNi(CO)4中含有σ键的数目为8NA.查看答案和解析>>
科目: 来源: 题型:解答题
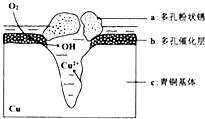 铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:
铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com