
科目: 来源: 题型:选择题
| A. | 容器内只含有18O2、SO2、SO3三种分子 | |
| B. | 18O只存在18O2分子中 | |
| C. | 容器内含有18O2、S18O2、S18O3等分子 | |
| D. | 反应达到限度时,所有物质的质量都相等 |
查看答案和解析>>
科目: 来源: 题型:解答题
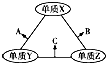 (Ⅰ) W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与Z相邻; X,Y位于同一主族,它们能组成YX2,YX3两种常见化合物;W元素的氢化物与Z元素的氢化物反应生成盐.请回答下列问题:
(Ⅰ) W,X,Y,Z四种短周期元素,原子序数依次增大,在周期表中W与X相邻、Y与Z相邻; X,Y位于同一主族,它们能组成YX2,YX3两种常见化合物;W元素的氢化物与Z元素的氢化物反应生成盐.请回答下列问题: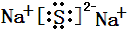 .(用元素符号表示)
.(用元素符号表示)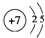 .
.查看答案和解析>>
科目: 来源: 题型:解答题
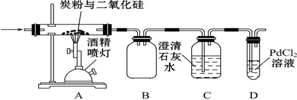
查看答案和解析>>
科目: 来源: 题型:解答题
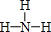 .
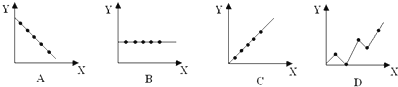
.
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | “另一种反应物”一定具有还原性 | B. | “另一种反应物”一定只具有氧化性 | ||
| C. | 2CuH+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl | D. | CuH既可作氧化剂也可作还原剂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| X | Y | ||
| Z | W | Q |
| A. | W得电子能力比Q强 | |
| B. | Z的氧化物能与水直接化合生成对应的酸 | |
| C. | 钠与Y可能形成的两种常见化合物阴阳离子个数比均为1:2 | |
| D. | X有多种同素异形体,而Y不存在同素异形体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③④ | B. | ②③④ | C. | ③④ | D. | ①②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{a}{m+A}$(A-N+m)mol | B. | $\frac{a}{A}$(A一N)mol | C. | $\frac{a}{m+A}$(A-N)mol | D. | $\frac{a}{A}$(A一N+m)mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀铜电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | 水玻璃中加入稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ | |
| C. | 在氯化铝溶液中滴加过量的氨水:Al3++3 OH-═Al (OH)3↓ | |
| D. | 大理石与盐酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单质能与水反应生成强碱的金属元素都在ⅠA族 | |
| B. | L层上的电子数为奇数的元素一定是主族元素 | |
| C. | 稀有气体元素原子的最外层电子数均为8 | |
| D. | 元素周期表有18个纵行,分列16个族,即7个主族、8个副族和一个零族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com