
科目: 来源: 题型:选择题
| A. | 甲烷燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 铝片与盐酸反应 | D. | 氧化钙与水反应 |
查看答案和解析>>
科目: 来源: 题型:实验题
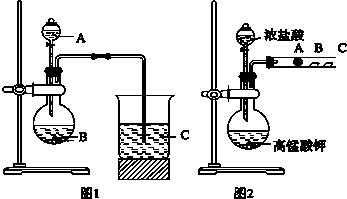
查看答案和解析>>
科目: 来源: 题型:解答题
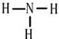
| I1 | I2 | I3 | I4 | I5 | I6 | |
| In | 578 | 1817 | 2745 | 11578 | 14831 | 18378 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ④ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ⑨ |
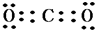 ,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为
,①、⑥两种元素能形成含共价键的离子化合物,该化合物的电子式为 ;用电子式表示元素③和⑨形成化合物的过程
;用电子式表示元素③和⑨形成化合物的过程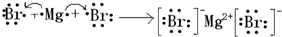
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | WX3和水反应形成的化合物是共价化合物 | |
| B. | 单质的熔点:Y>Z | |
| C. | X、Y、R形成的某种化合物可以用于漂白、消毒 | |
| D. | Y、Z和W三者最高价氧化物对应的水化物能两两相互反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| X | Y | ||
| W | Z | ||
| T |
| A. | 气态氢化物的稳定性:Y>W>X | |
| B. | X、Y两种元素形成的化合物只有两种 | |
| C. | 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2O在高温下也难分解 | |
| B. | F2、Cl2、Br2、I2单质的熔点依次升高 | |
| C. | SiH4的熔点高于CH4的熔点 | |
| D. | NH3的沸点高于PH3的沸点 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Y2分子中,σ键和π键数目之比为2:1 | |
| B. | Z单质与W单质发生反应,产物只有一种 | |
| C. | 元素X、Z形成的化合物中仅含极性共价键 | |
| D. | 只含X、Y、Z三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①④⑦⑧ | B. | ③④⑦⑧ | C. | ②⑤⑧⑨ | D. | ④⑦⑧⑨ |
查看答案和解析>>
科目: 来源: 题型:选择题
| X | Y | ||
| Z | W | Q |
| A. | 钠与W可以形成离子化合物Na2W2 | |
| B. | 由Z与Y组成的物质在熔融时能导电 | |
| C. | 氧化物对应水化物的酸性:Q>W | |
| D. | 固态XY2和ZY2的化学键类型、晶体类型都相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com