
科目: 来源: 题型:选择题
| A. | 离子化合物NH4Cl中既存在离子键,又存在极性共价键 | |
| B. | H2S的电子式是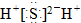 | |
| C. | 化学键包括离子键、共价键、氢键等 | |
| D. | LiOH、NaOH、KOH的碱性逐渐减弱 |
查看答案和解析>>
科目: 来源: 题型:选择题
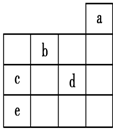
| A. | 元素b位于VIA族,有+6、-2两种常见化合价 | |
| B. | 元素的最高价氧化物对应的水化物的酸性:d>c>e | |
| C. | 金属性c>e | |
| D. | 元素的气态氢化物的稳定性:e>c>d |
查看答案和解析>>
科目: 来源: 题型:解答题
实验 混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO4(mL) | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液(mL) | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O(mL) | V7 | V8 | V9 | V10 | 10 | 0 |
| 实验序号 | 金属质量/g | 金属状态 | C(H2SO4)/mol.-L | V(H2SO4)/mL | 溶液温度 | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.1 | 丝 | 0.5 | 50 | 20 | 34 | 500 |
| 2 | 0.1 | 粉末 | 0.5 | 50 | 20 | 35 | 50 |
| 3 | 0.1 | 丝 | 0.7 | 50 | 20 | 36 | 250 |
| 4 | 0.1 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 5 | 0.1 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 6 | 0.1 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 7 | 0.1 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | SO2+2H2S═3S↓+2H2O | ||
| C. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 水玻璃中加入稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ | |
| B. | 铝与稀硝酸反应:2Al+6H+═2Al3++3H2↑ | |
| C. | 氯化铝溶液和过量氨水反应:Al3++3NH3•H2O═3NH4++Al (OH)3↓ | |
| D. | 向硅酸钠溶液中通入过量二氧化碳:SiO32-+CO2+H2O═H2SiO3↓+CO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径Y>Z>X>W | B. | 氢化物的稳定性H2Y>HZ | ||
| C. | 离子的氧化性aW3+>bX+ | D. | a+3<c-2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X:氯化铝溶液,Y:氨气 | |
| B. | X:硅酸钠溶液,Y:二氧化硫 | |
| C. | X:氢氧化钡溶液,Y:一氧化碳 | |
| D. | X:四羟基合铝酸钠溶液,Y:二氧化氮 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 工业上生产水泥和玻璃都要用石灰石做原料 | |
| B. | 玻璃钢是一种合金材料 | |
| C. | 除去氨气中的水蒸气可用无水氯化钙可做干燥剂 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用氯化铝和纯硝酸反应 | |
| B. | 氯化铝与氢氧化钠反应,过滤得沉淀,再加稀HNO3 | |
| C. | 用AlCl3溶液和氨水反应,过滤得沉淀,再加稀HNO3 | |
| D. | AlCl3溶液和Ba(NO3)2溶液反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 任何化学反应都伴随着能量的变化 | |
| B. | H2O(气)-→H2O(液)该过程放出大量的热,所以该过程是化学变化 | |
| C. | 化学反应中能量的变化都表现为热量的变化 | |
| D. | 所有的物质一定存在化学键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com