
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ž¢ß | B£® | ¢Ū¢Ż¢ß | C£® | ¢Ū¢Ž¢ß | D£® | ¢Ś¢Ū¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
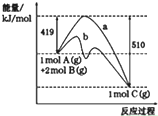
| A£® | ĒśĻßb±ķŹ¾Ź¹ÓĆ“ß»Æ¼ĮŗóµÄÄÜĮæ±ä»Æ | |
| B£® | Õż·“Ó¦»ī»ÆÄÜ“óÓŚÄę·“Ó¦»ī»ÆÄÜ | |
| C£® | ÓÉĶ¼æÉÖŖøĆ·“Ó¦µÄģŹ±ä”÷H=+91 kJ•mol-1 | |
| D£® | ·“Ó¦ÖŠ½«ĘųĢåA»»ĪŖ¹ĢĢå·“Ó¦£¬ĘäĖūĢõ¼ž²»±ä£¬·“Ó¦·Å³öČČĮæ“óÓŚ91kJ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«0.5molN2ŗĶ1.5molH2³äČėŅ»ĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦£¬·Å³öČČĮæ19.6KJŌņøĆČČ»Æѧ·½³ĢŹ½ĪŖN2£Øg£©+3 H2£Øg£©?2NH3£Øg£©”÷H=-39.2 KJ•mol-1 | |
| B£® | ÓÉC£ØŹÆÄ«£©=C£Ø½šøÕŹÆ£©£»”÷H=+1.9 kJ/mol£¬æÉÖŖ½šøÕŹÆ±ČŹÆÄ«ĪČ¶Ø | |
| C£® | ŌŚĻ”ČÜŅŗÖŠ£ŗH+£Øaq£©+OH-£Øaq£©=H2O£Øl£©£»”÷H=-57.3kJ/mol£¬Ōņŗ¬40.0 g NaOHµÄĻ”ČÜŅŗÓėĻ”“×ĖįĶźČ«ÖŠŗĶ£¬·Å³öŠ”ÓŚ57.3 kJµÄČČĮæ | |
| D£® | ŌŚ101kPaŹ±£¬2gH2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®£¬·Å³ö285.8kJČČĮ棬ĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ£ŗ2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H=-285.8kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ±5NAøöµē×Ó×ŖŅĘŹ±£¬øĆ·“Ó¦·Å³ö650 kJµÄČČĮæ | |
| B£® | µ±1NAøöĖ®·Ö×ÓÉś³ÉĒŅĪŖĘųĢåŹ±£¬·Å³ö¶ąÓŚ1300 kJµÄČČĮæ | |
| C£® | µ±2 NAøöĢ¼ŃõĖ«¼üÉś³ÉŹ±£¬·Å³ö1300 kJµÄČČĮæ | |
| D£® | µ±4NAøöĢ¼Ńõ¹²ÓƵē×Ó¶ŌÉś³ÉŹ±£¬·Å³ö1300kJµÄČČĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Õż¼«ĪŖCu£¬øŗ¼«ĪŖFe£¬µē½āÖŹĪŖFeCl3ČÜŅŗ | |
| B£® | øŗ¼«ĪŖFe£¬Õż¼«ĪŖC£¬µē½āÖŹĪŖFe£ØNO3£©2ČÜŅŗ | |
| C£® | Õż¼«ĪŖAg£¬øŗ¼«ĪŖFe£¬µē½āÖŹĪŖFe2£ØSO4£©3ČÜŅŗ | |
| D£® | øŗ¼«ĪŖFe£¬Õż¼«ĪŖPt£¬µē½āÖŹĪŖFe2£ØSO4 £©3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
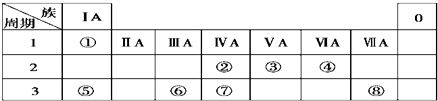
| A£® | Ö»ÓŠ¢Ł | B£® | ¢Ś¢Ü | C£® | ¢Ł¢Ś¢Ü | D£® | ¢Ł¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ū | B£® | ¢Ł¢Ž | C£® | ¢Ü¢Ž | D£® | ¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«“æĖ®¼ÓČČ£¬ĘäKWŌö“ó¶ųPH²»±ä | |
| B£® | ³£ĪĀĻĀ£¬PH=6µÄČÜŅŗŅ»¶ØŹĒĖįČÜŅŗ | |
| C£® | 25”ꏱ£¬0.1mol/µÄĮņ»ÆĒāČÜŅŗ±ČµČÅØ¶ČµÄĮņ»ÆÄĘČÜŅŗµÄµ¼µēÄÜĮ¦Čõ | |
| D£® | Ļņ°±Ė®ÖŠ¼ÓČėĀČ»Æļ§¹ĢĢå»įŹ¹ČÜŅŗµÄpHŌö“ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com