
科目: 来源: 题型:选择题
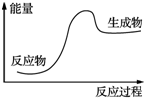
| A. | 铝热反应 | B. | 氧化钙和水反应 | ||
| C. | C+H2O$\stackrel{高温}{→}$CO+H2 | D. | 一氧化碳气体的燃烧 |
查看答案和解析>>
科目: 来源: 题型:解答题
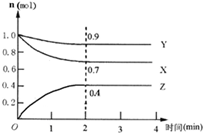 某可逆反应在某体积为5L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X、Y、Z均为气体).
某可逆反应在某体积为5L的密闭容器中进行,在从0~4分钟各物质的量的变化情况如图所示(X、Y、Z均为气体).查看答案和解析>>
科目: 来源: 题型:解答题
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
查看答案和解析>>
科目: 来源: 题型:选择题
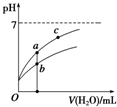 25℃时某些弱酸的电离平衡常数如下表所示:
25℃时某些弱酸的电离平衡常数如下表所示:| CH3COOH | HClO | H2CO3 |
| K(CH3COOH) =1.8×10-5 | K(HClO) =3.0×10-8 | K(H2CO3)a1=4.4×10-7 K(H2CO3)a2=4.7×10-11 |
| A. | 相同浓度的CH3COOH和HClO的混合溶液中,各离子浓度的大小关系是:c(H+)>c(ClO-)>c(CH3COO-)>c(OH-) | |
| B. | 图象中a、c两点所处的溶液中$\frac{c({R}^{-})}{c(HR)•c(O{H}^{-})}$相等(HR代表CH3COOH或HClO) | |
| C. | 图象中a点酸的浓度大于b点酸的浓度 | |
| D. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32- |
查看答案和解析>>
科目: 来源: 题型:选择题
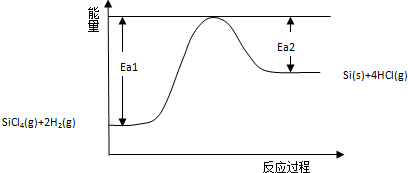
| A. | 反应过程中,若通过缩小体积增大压强,则活化分子百分数变大,反应速率加快 | |
| B. | 若Si-Cl、H-H、Si-Si、H-Cl的键能分别为Ea、Eb、Ec、Ed(单位:),则△H=(4Ea+2Eb-Ec-4Ed )KJ/mol | |
| C. | 该反应能量变化如图所示,则Ea1、Ea2分别代表该反应正向和逆向的活化能,使用催化剂Ea1、Ea2都减小,△H也变小 | |
| D. | 由如图和题目信息可知该反应△H>0,△S>0,所以在较高温度下可自发进行 |
查看答案和解析>>
科目: 来源: 题型:选择题
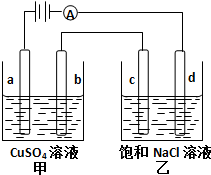
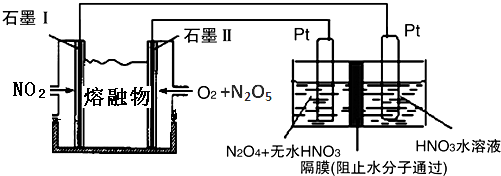
| A. | 甲中a的电极反应为:4OH--4e-=O2↑+2H2O | |
| B. | 电解时向乙中滴入酚酞试剂,c电极附近先变红 | |
| C. | 当d电极产生2g气体时,b极有32g物质析出 | |
| D. | 电解少量时间后向乙中加适量盐酸,溶液组成可以恢复到原电解前的状态 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | N2(g)+3H2(g)?2NH3(g);△H<0 | B. | 2SO3(g)?2SO2(g)+O2(g);△H>0 | ||
| C. | 4NH3(g)+5O2(g)?4NO+6H2O(g);△H<0 | D. | CO(g)+2H2(g)?CH3OH(g)△H<0 |
查看答案和解析>>
科目: 来源: 题型:选择题
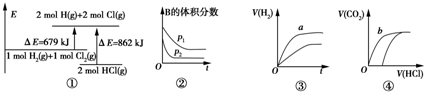
| A. | ①表示化学反应H2(g)+Cl2(g)═2HCl(g)的能量变化,则该反应的反应热△H=+183 kJ/mol | |
| B. | ②表示其他条件不变时,反应4A(g)+3B(g)═2C(g)+6D在不同压强下B的体积分数随时间的变化,则D一定是气体 | |
| C. | ③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | ④表示10 mL 0.1 mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.1 mol/L盐酸,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 正、逆反应速率相等且都等于零 | |
| B. | c(A2):c(B2):c(AB)=1:1:2 | |
| C. | A2、B2和AB的物质的量不再改变 | |
| D. | 单位时间内消耗n mol A2的同时生成2n mol AB |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com