
科目: 来源: 题型:选择题
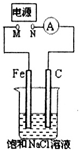
| A. | M连接电源正极,N连接电源负极,当两极产生气体总量为22.4mL(标准状况)时,则生成0.001molNaOH | |
| B. | 去掉电源,将M、N用导线直接相连,在溶液中滴入酚酞试液,C电极周围溶液变红 | |
| C. | M连接电源负极,N连接电源正极,如果把烧杯中的溶液换成1LCuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 | |
| D. | M连接电源正极,N连接电源负极,将C电极换成Cu电极,电解质溶液换成硫酸铜溶液,则可实现在铁上镀铜 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 放电时NaTi2(PO4)3在正极发生还原反应 | |
| B. | 放电时负极材料中的Na+脱离电极进入溶液,同时溶液中的Na+嵌入到正极材料中 | |
| C. | 充电过程中阳极反应式为:2NaNiFeIIⅢ(CN)6+2Na++2e-=2Na2NiFeⅡ(CN)6 | |
| D. | 该电池在较长时间的使用过程中电解质溶液中Na+的浓度基本保持不变 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 钢管与铅连接,钢管可被保护 | |
| B. | 铁遇冷浓硫酸表面钝化,可保护内部不被腐蚀 | |
| C. | 纯铁比生铁更容易被腐蚀 | |
| D. | 钢铁发生析氢腐蚀时,负极反应是Fe-3e-═Fe3+ |
查看答案和解析>>
科目: 来源: 题型:解答题
| 温度(℃) 气体总浓度 (mol/L) 时间(min) | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 9×10-3 | 2.7×10-2 | 8.1×10-2 |
| t2 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |
| t3 | 3×10-2 | 4.8×10-2 | 9.4×10-2 |

查看答案和解析>>
科目: 来源: 题型:解答题
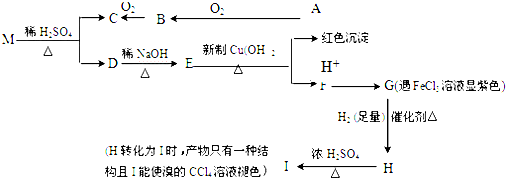
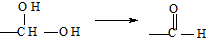
 ;②H→I:
;②H→I: .
. .
.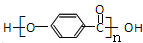 .
. 等.(任写一种)
等.(任写一种)查看答案和解析>>
科目: 来源: 题型:解答题
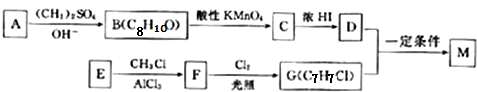
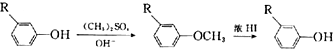
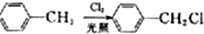
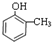 ;E→F的反应类型为取代反应.
;E→F的反应类型为取代反应.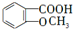 +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$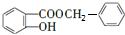 +HCl
+HCl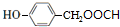 (写结构简式).
(写结构简式). 和(CH2)3CCl为起始原料制备
和(CH2)3CCl为起始原料制备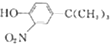 的合成路线:
的合成路线: $→_{AlCl_{3}}^{(CH_{3})_{3}CCl}$
$→_{AlCl_{3}}^{(CH_{3})_{3}CCl}$ $→_{OH-}^{(CH_{3})_{2}SO_{4}}$
$→_{OH-}^{(CH_{3})_{2}SO_{4}}$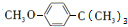 $→_{浓H_{2}O_{4}/△}^{浓HNO_{3}}$
$→_{浓H_{2}O_{4}/△}^{浓HNO_{3}}$ $\stackrel{浓HI}{→}$
$\stackrel{浓HI}{→}$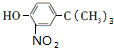 .
.查看答案和解析>>
科目: 来源: 题型:解答题


查看答案和解析>>
科目: 来源: 题型:选择题
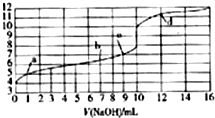
| A. | HA为一元强酸 | |
| B. | 水的电离程度:a点>b点>c点 | |
| C. | c点时,酸和碱恰好完全反应 | |
| D. | d点时,溶液中离子浓度:c(Na+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
科目: 来源: 题型:选择题
 图甲是在微生物的作用下将有机废水(主要含有葡萄糖)的化学能转化为电能的装置,图乙是用情性电极电解饱和食盐水制取一种家用消毒液的装置,下列说法错误的是( )
图甲是在微生物的作用下将有机废水(主要含有葡萄糖)的化学能转化为电能的装置,图乙是用情性电极电解饱和食盐水制取一种家用消毒液的装置,下列说法错误的是( )| A. | M电极的电极反应式为:C6H12O6-24e-+6H2O═6CO2↑+24H+ | |
| B. | N电极上每消耗22.4L气体(标准状况)时,则有4molH+通过质子交换膜从负极区移向正极区 | |
| C. | 若装置乙所需的电能来自装置甲,则b极应与X极连接 | |
| D. | 由装置乙制得的家用消毒液的有效成分是NaClO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com