
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
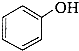
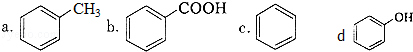
 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.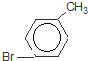 或
或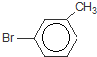 或
或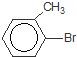 .
.查看答案和解析>>
科目: 来源: 题型:选择题
 我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )| A. | 该物质属于芳香族化合物 | |
| B. | 该有机物的分子式为C15H18O3 | |
| C. | 遇FeCl3溶液呈紫色,因为该物质与苯酚属于同系物 | |
| D. | 1mol该化合物最多可与含3molBr2的溴水发生反应 |
查看答案和解析>>
科目: 来源: 题型:解答题


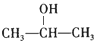 +NaCl;
+NaCl;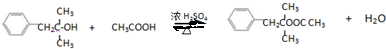 ;
;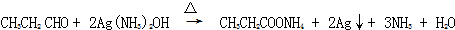 .
.查看答案和解析>>
科目: 来源: 题型:解答题
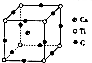 短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层能级中有3个未成对电子.
短周期元素A、B、C、D,A元素的原子最外层电子排布式为ms1,B元素的原子价电子排布式为ns2np2,C元素位于第二周期且原子中p能级与所有s能级电子总数相等,D元素原子的L层能级中有3个未成对电子.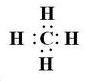 ,BC2属于非极性分子(填”极性“或”非极性“);当n=3时,B与C形成的晶体属于原子晶体.
,BC2属于非极性分子(填”极性“或”非极性“);当n=3时,B与C形成的晶体属于原子晶体.查看答案和解析>>
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 5:6 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 电池工作室,锂电极反应式为Li-e-═Li+ | |
| B. | 若将石墨换成铁时,电池还能继续工作 | |
| C. | 电池工作时,电解质中的ClO4-运动到电池的石墨极 | |
| D. | 正极发生了还原反应 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 分子式为C16H16O9 | |
| B. | 能与碳酸钠溶液反应,但不产生二氧化碳 | |
| C. | 能发生催化氧化反应并生成能发生银镜反应的产物 | |
| D. | NaOH、H2、溴水分别与1mol绿原酸反应时,消耗反应物的最大物质的量都为4mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 食品包装中的干燥剂必须用特别包装纸包装,其成分多为氧化钙颗粒,也有硅胶颗粒 | |
| B. | 蛋白质、塑料、合成橡胶、光导纤维都是高分子化合物 | |
| C. | Fe2O3、CuO、PbO等金属氧化物是我国古代就已经使用的用于烧碱釉陶的彩色釉面原料 | |
| D. | 控制汽车尾气、工业尾气、建筑扬尘、垃圾焚烧等的任意排放是治理雾霾天气重要环节 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com