
科目: 来源: 题型:选择题
| A. | KOH和CaCl2既含有离子键,又含有共价键 | |
| B. | PH3各原子均满足8电子稳定结构 | |
| C. | 硫离子的结构示意图: | |
| D. | NH4Cl的电子式: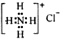 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
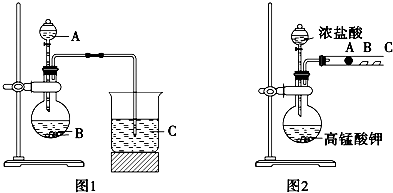
| 验证化学能转化为电能 | 验证非金属性:Cl>C>Si | 实验室制氨气 | 研究催化剂对化学反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | b、a、d、c、e | B. | e、b、a、d、c | C. | c、b、e、a、b | D. | b、a、e、d、c |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | WX2、WZ2分子中所有原子最外层都为8电子结构 | |
| B. | WX2、ZX2的化学键类型和晶体类型都相同 | |
| C. | X的氢化物的熔沸点比Z的氢化物的熔沸点高 | |
| D. | 原子半径大小顺序为X<W<Y<Z |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
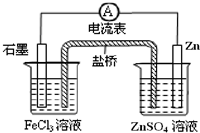 根据下列原电池示意图,回答下列问题:
根据下列原电池示意图,回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素周期表揭示了化学元素间的内在联系,是化学发展史上重要里程碑 | |
| B. | 在周期表中,把电子层数相同的元素排成一横行,称为一周期 | |
| C. | 元素周期表中,总共有18个纵行,18个族,IIIB族含有32种金属元素 | |
| D. | 第IA族(除H)元素又称为碱金属元素,第ⅦA族元素又称为卤族元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com