
科目: 来源: 题型:选择题
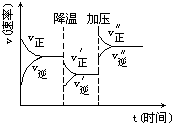 图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A. | A、B、C、D均为气体 | B. | 若A、B是气体,则C、D是液体或固体 | ||
| C. | 逆反应是放热反应 | D. | 在整个过程中,A的转化率一直增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 使用适当的催化剂只改变正反应速率 | |
| B. | 降低压强能提高逆反应速率 | |
| C. | 升高温度能同时提高正、逆反应速率 | |
| D. | 减小压强对正反应速率影响小于逆反应速率的影响 |
查看答案和解析>>
科目: 来源: 题型:解答题
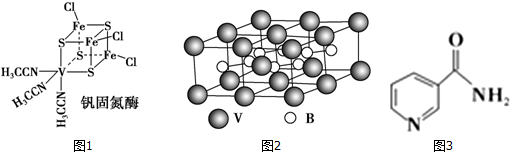
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题


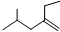 的系统命名4-甲基-2-乙基-1-戊烯
的系统命名4-甲基-2-乙基-1-戊烯查看答案和解析>>
科目: 来源: 题型:选择题
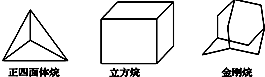
| A. | 2种,4种,8种 | B. | 2种,4种,6种 | C. | 1种,3种,6种 | D. | 1种,3种,8种 |
查看答案和解析>>
科目: 来源: 题型:解答题
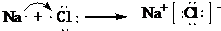
查看答案和解析>>
科目: 来源: 题型:解答题
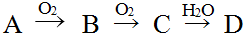
查看答案和解析>>
科目: 来源: 题型:解答题
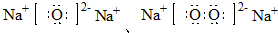 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 第二周期 IVA族 | B. | 第三周期 IV A族 | C. | 第三周期 VI A族 | D. | 第二周期VI A族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com