
科目: 来源: 题型:选择题
| A. | 平衡体系中氮气、氢气、氨的物质的量保持不变 | |
| B. | 平衡体系中氮气、氢气、氨的浓度保持不变 | |
| C. | 单位时间内生成的氨和分解的氨物质的量相同 | |
| D. | 单位时间内消耗的氮气和氢气与生成的氨气物质的量相同 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 偏二甲肼既是氧化剂又是还原剂 | |
| B. | 该反应进行时只有放热过程没有吸热过程 | |
| C. | 该反应中氮元素的化合价升高 | |
| D. | 该反应中每生成1mol CO2转移8mol电子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 56g Fe与稀HNO3完全反应时一定转移3NA个电子 | |
| B. | 标准状况下11.2 L NH3溶于1 L水中,溶液中含N原子的微粒总数为0.5NA | |
| C. | 常温常压下,0.1NA个Al与足量氢氧化钠溶液反应生成3.36 LH2 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
查看答案和解析>>
科目: 来源: 题型:解答题
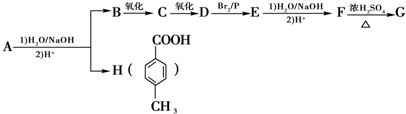
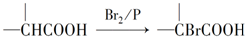
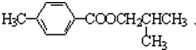 .
.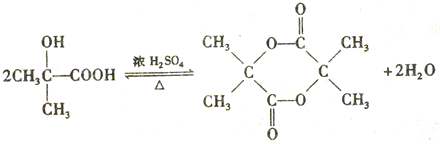 .
.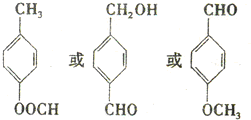 .
. )结构.
)结构.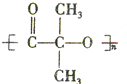 ,形成该聚合物的反应类型为:缩聚反应.
,形成该聚合物的反应类型为:缩聚反应.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

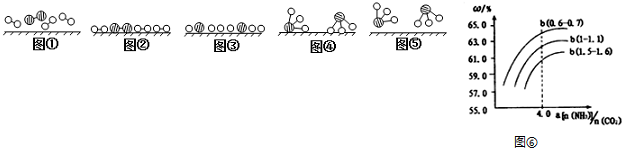
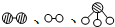 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面、在催化剂表面N2、H2中化学键断裂.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com