
科目: 来源: 题型:选择题

| A. | 用水润湿的 pH 试纸测量某溶液的 pH | |
| B. | 用量筒量取 20 mL 0.5000 mol/LH2SO4溶液于烧杯中,加水 80 mL,配制成 0.1000 mol/LH2SO4溶液 | |
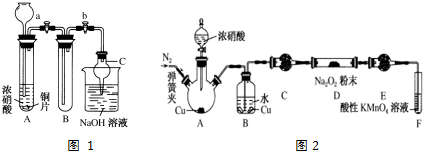
| C. | 实验室用图Ⅰ所示装置制取并收集少量氨气 | |
| D. | 实验室用图Ⅱ所示装置除去Cl2中的少量HCl |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该电池充电时,锂极与外电源的负极相连 | |
| B. | 该电池放电时,Li+向负极移动 | |
| C. | 该电池充电时阴极的反应为LixV2O4-xe-=V2O4+xLi+ | |
| D. | 若放电时转移 0.2 mol 电子,则消耗锂 1.4x g |
查看答案和解析>>
科目: 来源: 题型:选择题
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的$\frac{2}{3}$ |
| Z | 第三周期原子半径最小的金属元素 |
| A. | 气态氢化物的热稳定性:X>W | |
| B. | 最高价氧化物对应水化物的酸性:Y>X | |
| C. | 离子半径:Z>W | |
| D. | Z 的氧化物不具有两性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 问题 | 评价 |
| A | 用稀硝酸清洗做过银镜反应的试管 Ag+4H++NO3-=Ag++NO↑+2H2O | 错误,物质拆分错误 |
| B | 离子组 Na+、K+、HCO3-、OH- | 不能大量共存于同一溶液中,因为发生反应: HCO3-+OH-=H2O+CO2↑ |
| C | 反应: Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq) | 该反应的平衡常数表达式:K=$\frac{{K}_{sp}(MnS)}{{K}_{sp}(CuS)}$ |
| D | 在硫酸氢钠溶于水的过程中 | 只有离子键被破坏没有共价键被破坏 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 拉瓦锡研究了空气的成分,让大家认识了氧气 | |
| B. | 图为雾霾的主要成分示意图,汽车尾气的大量排放是造成雾霾天气的人为因素之一 | |
| C. | “滴水石穿、绳锯木断、落汤螃蟹着红袍”均不包含化学变化 | |
| D. | “看似风平浪静,实则暗流涌动”形象地描述了溶解平衡的状态 |
查看答案和解析>>
科目: 来源: 题型:解答题
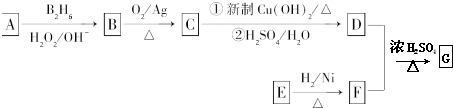
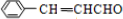 .
.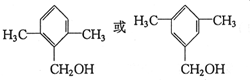 .
.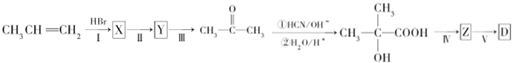
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分散系中分散质粒子的大小:Fe(OH)3悬浊液<Fe(OH)3胶体<FeCl3溶液 | |
| B. | 焰色反应是物质燃烧时火焰呈现的颜色变化,属于化学变化 | |
| C. | 生石灰用作食品抗氧剂 | |
| D. | “海水淡化”可以解决“淡水供应危机”,但加入明矾不能使海水淡化 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com