
科目: 来源: 题型:解答题
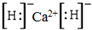 .
.查看答案和解析>>
科目: 来源: 题型:解答题


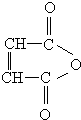 .
.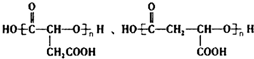 .
.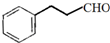 )与F的相对分子质量相同,其中满足下列条件的X的同分异构体有14种(含X本身).
)与F的相对分子质量相同,其中满足下列条件的X的同分异构体有14种(含X本身). 的最简合成线路.
的最简合成线路.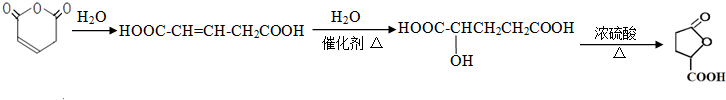 .
.查看答案和解析>>
科目: 来源: 题型:解答题
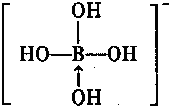 .(若存在配位键需标出)
.(若存在配位键需标出)
查看答案和解析>>
科目: 来源: 题型:选择题
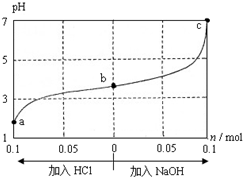
| A. | a、b、c 对应的混合液中,水的电离程度由大到小的顺序的是a>b>c | |
| B. | c点混合液中c(Na+)>c(CH3COO-) | |
| C. | 加入NaOH过程中,$\frac{c(N{a}^{+})×c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$减小 | |
| D. | 若忽略体积变化,则25℃时CH3COOH的电离平衡常数 K=$\frac{0.2}{w-0.2}$×10-7 mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
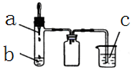 利用如图所示装置进行下列实验,实验现象与结论均正确的是( )
利用如图所示装置进行下列实验,实验现象与结论均正确的是( )| 选项 | 实验试剂 | 实验现象 | 实验结论 | ||
| a | b | c | |||
| A | 浓氨水 | 碱石灰 | FeCl2溶液 | 产生白色沉淀,迅速变为灰绿色,最后变为红褐色 | 氨气具有氧化性 |
| B | 稀硫酸 | FeS | AgCl悬浊液 | 悬浊液由白色变为黑色 | Ksp(AgCl)>Ksp(Ag2S) |
| C | 浓硝酸 | 铜 | BaSO3悬浊液 | 悬浊液变澄清 | +4价硫具有还原性 |
| D | 浓盐酸 | KMnO4 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2有酸性和漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
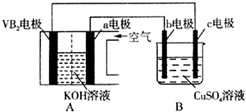 碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5.用该电池电解200mL硫酸铜溶液,实验装置如图所示(b、c均为惰性电极),当外电路中通过0.04mol电子时,B装置两极共收集到0.448L气体(标准状况).下列说法正确的是( )
碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5.用该电池电解200mL硫酸铜溶液,实验装置如图所示(b、c均为惰性电极),当外电路中通过0.04mol电子时,B装置两极共收集到0.448L气体(标准状况).下列说法正确的是( )| A. | 电解过程中,b电极表面先有红色物质析出,然后有气泡产生 | |
| B. | VB2为负极,电极反应为:2VB2+11H2O-22e-=V2O5+2B2O3+22H+ | |
| C. | 电池内部OH-移向a电极,溶液pH减小 | |
| D. | 忽略溶液体积变化,电解后B装置中溶液的pH为1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径:Z>G>M>Y | |
| B. | X、M形成的简单阴离子的还原性:X>M | |
| C. | G与Y形成的化合物一定既能与盐酸反应,又能与烧碱溶液反应 | |
| D. | X、Z分别与Y可形成原子数为1:1的物质 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 分子中所有碳原子可能共平面 | |
| B. | 既能发生酯化反应又能发生氧化反应 | |
| C. | 1 mol该物质与H2完全加成,需消耗3 mol H2 | |
| D. | 比该物质少一个O原子,属于芳香族化合物的同分异构体有2种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 22.4 L O2和O3的混合气中氧原子数为0.2NA | |
| B. | 标准状况下,22.4 L苯的分子数为NA | |
| C. | 46 g乙醇中含有的共价键总数为8 NA | |
| D. | 1 L 0.1 mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 明矾可作净水剂,向海水中加入明矾可以使海水淡化 | |
| B. | 离子交换膜在工业上应用广泛,在氯碱工业中使用阳离子交换膜 | |
| C. | 臭氧是一种氧化性较强的气体,可用于自来水的消毒 | |
| D. | SO2具有还原性,可用已知浓度的KMnO4溶液测定食品中SO2残留量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com