
科目: 来源: 题型:选择题
| A. | 正极附近的 SO4 2- 离子浓度逐渐增大 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 溶液的pH逐渐变小 | |
| D. | 铜片上有 H2 逸出 |
查看答案和解析>>
科目: 来源: 题型:解答题
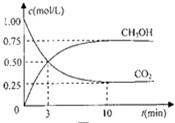 甲醇(CH3OH)是一种优质燃料,
甲醇(CH3OH)是一种优质燃料,查看答案和解析>>
科目: 来源: 题型:解答题
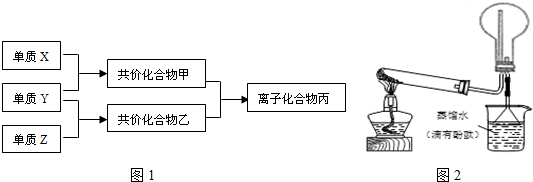
 ;甲的电子式:
;甲的电子式: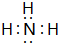 ;
;查看答案和解析>>
科目: 来源: 题型:解答题
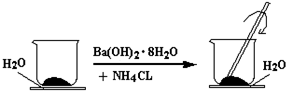
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 干冰升华克服了分子间作用力,没有破坏共价键 | |
| B. | HCl气体溶于水,形成稀盐酸,仅克服分子间作用力 | |
| C. | C60与金刚石互为同素异形体,它们都属于原子晶体 | |
| D. | 乙醇和二甲醚分子都是C2H6O,它们是同位素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | C | |
| B |
| A. | A为VB族元素 | |
| B. | B为第二周期的元素 | |
| C. | 三种元素都为金属元素 | |
| D. | C元素单质是化学性质最活泼的非金属 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 范德华力、范德华力 | B. | 范德华力、共价键 | ||
| C. | 共价键、范德华力 | D. | 共价键、共价键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com