
科目: 来源: 题型:选择题
| A. | Y、Z、W三种元素组成化合物的化学式可能为ZWY | |
| B. | Z与Y、Z与W形成的化合物的化学键类型可能完全相同 | |
| C. | 简单离子的半径:R>W>Y>Z | |
| D. | 因非金属性Y>R,所以X与Y组成化合物的沸点低于X与R组成的化合物 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 向CuSO4溶液中加入Na2O2:2Na2O2+Cu2++H2O═4 Na++Cu(OH)2↓+O2↑ | |
| B. | 工业上用石灰乳制备漂白粉:Ca+2OH-+Cl2=Ca2++ClO-+Cl-+H2O | |
| C. | 向Na2SiO3溶液中通入过量SO2:SiO32-+2SO2+2H2O═H2SiO3↓+2HSO3- | |
| D. | 制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 类比对象 | 结论 |
| A | 2F2+2H2O═4HF+O2 | 2I2+H2O═4HI+O2↑ |
| B | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | 3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ |
| C | Na2O+H2O═2NaOH | FeO+H2O═Fe(OH)2 |
| D | Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O═CaSO3↓+2HClO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
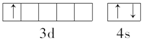 ,该元素基态原子结构示意图
,该元素基态原子结构示意图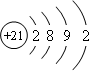 .该元素的名称为钪,形成的单质为金属晶体.
.该元素的名称为钪,形成的单质为金属晶体. 中心原子的杂化方式为
中心原子的杂化方式为查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金刚石的网状结构中,由共价键形成的碳原子环,其中最小的环上有6个碳原子 | |
| B. | 在氯化钠晶体中,每个Na+或Cl-的周围紧邻6个Cl-或6个Na+ | |
| C. | 干冰晶体熔化时,1mol干冰要断裂2mol碳氧双键 | |
| D. | 在氯化铯晶体中,每个Cs+周围紧邻8个Cl-,每个Cl-周围也紧邻8个Cs+ |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:推断题
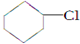 (一氯环己烷)$→_{△②}^{NaOH、乙醇}$
(一氯环己烷)$→_{△②}^{NaOH、乙醇}$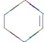 $→_{③}^{Br_{2}的CCl_{4}溶液}$B $\stackrel{④}{→}$
$→_{③}^{Br_{2}的CCl_{4}溶液}$B $\stackrel{④}{→}$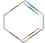
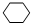 ,名称是环己烷.
,名称是环己烷.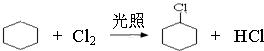 、
、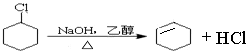 .
.查看答案和解析>>
科目: 来源: 题型:解答题
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com