
科目: 来源: 题型:选择题
| A. | 反应不需要加热即可进行反应 | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 反应物的总键能高于生成物的总键能 | |
| D. | 理论上可以使该反应的化学能直接转化为电能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ${\;}_{83}^{209}$Bi比${\;}_{83}^{210}$Bi的质量数小1 | |
| B. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi都含有83个中子 | |
| C. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi的核外电子数不同 | |
| D. | ${\;}_{83}^{209}$Bi和${\;}_{83}^{210}$Bi分别含有126和127个质子 |
查看答案和解析>>
科目: 来源: 题型:解答题
 .
.查看答案和解析>>
科目: 来源: 题型:解答题
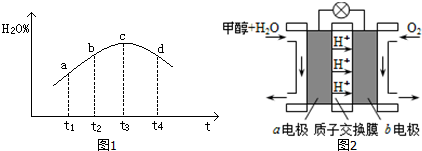
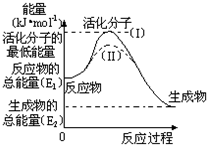 在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示.请认真观察如图,然后回答问题.
在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子.使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJ•mol-1表示.请认真观察如图,然后回答问题.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 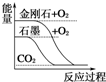 石墨转变成金刚石是吸热反应 | |
| B. | 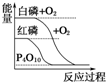 白磷比红磷稳定 | |
| C. | 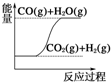 CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 | |
| D. | 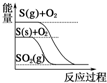 S(g)+O2(g)═SO 2(g)△H1 S(g)+O2((g)═SO2((g)△H2,则△H1>△H2 |
查看答案和解析>>
科目: 来源: 题型:解答题
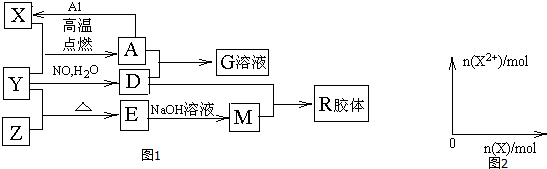
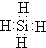 .
.查看答案和解析>>
科目: 来源: 题型:解答题
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | - |
查看答案和解析>>
科目: 来源: 题型:填空题
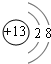 .
. ;
;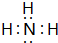 ,G的结构式为
,G的结构式为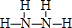 .
.查看答案和解析>>
科目: 来源: 题型:选择题
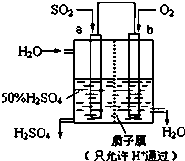
| A. | a为负极,b为正极 | |
| B. | b电极发生氧化反应 | |
| C. | H+从a极向b极移动 | |
| D. | 负极反应式为:SO2+2H2O-2e-=SO42-+4H+ |
查看答案和解析>>
科目: 来源: 题型:选择题
 某实验小组对一含有Al3+的未知溶液进行了如下分析:
某实验小组对一含有Al3+的未知溶液进行了如下分析:| A. | 该未知溶液中一定含有Al3+ Mg2+ H+三种阳离子 | |
| B. | 滴加的NaOH溶液的物质的量浓度为5 mol•L-1 | |
| C. | 若将最终沉淀过滤、洗涤、灼烧,其质量可能为6 g | |
| D. | 若另一种离子为二价阳离子,则a=10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com