
科目: 来源: 题型:选择题
| A. | “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 | |
| B. | 碘是人体必需微量元素,所以要多吃富含高碘酸的食物 | |
| C. | 药皂中含有苯酚,能杀菌消毒,故苯酚具有强氧化性 | |
| D. | 屠呦呦获得了2015年诺贝尔奖,她用乙醚提取青蒿素的过程属于化学变化 |
查看答案和解析>>
科目: 来源: 题型:解答题
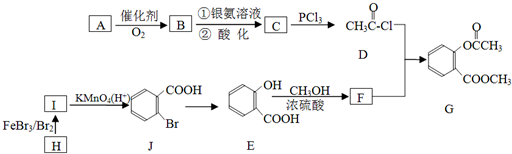
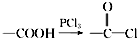 ,请回答以下问题:
,请回答以下问题: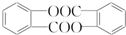 .
.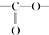 结构
结构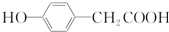 .
.查看答案和解析>>
科目: 来源: 题型:多选题
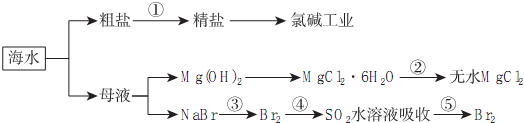
| A. | 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 在过程④中SO2被氧化 | |
| C. | 从第③步到第⑤步的目的是为了浓缩 | |
| D. | 从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
查看答案和解析>>
科目: 来源: 题型:多选题
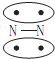 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示π键,下列说法中不正确的是 ( )
,其中椭圆框表示π键,下列说法中不正确的是 ( )| A. | N2分子与CO分子中都含有叁键 | |
| B. | CO分子中有一个π键是配位键 | |
| C. | N2、CO分别由非极性键和极性键结合,因此二者不是等电子体 | |
| D. | N2与CO的化学性质相同 |
查看答案和解析>>
科目: 来源: 题型:解答题
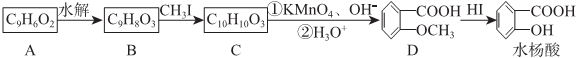
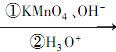 RCOOH+R1COOH
RCOOH+R1COOH .
.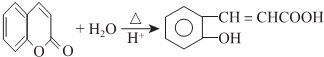 .
.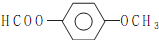 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X、Y间可形成离子化合物 | |
| B. | 单质熔点:Y>W>X | |
| C. | 最高价氧化物对应水化物的酸性:Z>W | |
| D. | Y、W形成的单核离子均能破坏水的电离平衡 |
查看答案和解析>>
科目: 来源: 题型:选择题
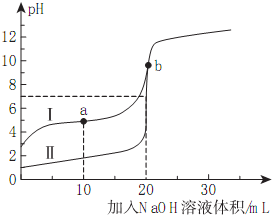 室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是( )
室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的HA和HB溶液,滴定曲线如图所示.下列说法错误的是( )| A. | 当Ⅰ代表HB,b点时体系中有:c(B-)+c(HB)=0.05mol/L | |
| B. | 滴定分析中,甲基橙不能用做滴定曲线Ⅰ中的指示剂 | |
| C. | a点时的溶液中离子浓度最大的是c(Na+) | |
| D. | 若Ⅱ代表HA的滴定曲线,则Ka(HB)≈10-5 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 上述灼烧过程的尾气回收后可用来制硫酸 | |
| B. | 上述过程中,由6molCuFeS2制取6molCu时共消耗15molO2 | |
| C. | 在反应2Cu2O+Cu2S=6Cu+SO2↑中,氧化产物与还原产物的物质的量比1:6 | |
| D. | 在反应2Cu2O+Cu2S=6Cu+SO2↑中,只有Cu2O作氧化剂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A | B | C | D | |
| 装置 | 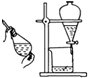 | 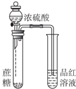 | 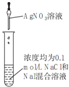 | 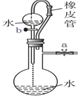 |
| 目的 | 用NaOH溶液除去溴苯中单质溴 | 证明浓硫酸有脱水性、强氧化性 | 确定Ksp(AgCl)、Ksp(AgI)的相对大小 | 观察水能否全部流下判断装置气密性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com