
科目: 来源: 题型:选择题
| A. | 浓硫酸使胆矾晶体变白(脱水性) | |
| B. | 在加热条件下铜与浓硫酸反应(氧化性、酸性) | |
| C. | 蔗糖与浓硫酸反应中有海棉状的炭生成(吸水性) | |
| D. | 浓硫酸可用来干燥某些气体(不挥发性) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1L 1mol•L-1的NaClO溶液含有ClO-的数目为NA | |
| B. | 22.4 L Cl2分别与足量的Cu、Fe完全反应转移电子数分别为2NA、3NA | |
| C. | 常温常压下,14g由N2和CO组成的混合气体含有的电子总数为7NA | |
| D. | 14.2g硫酸钠固体含有0.l NA个硫酸钠分子 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题
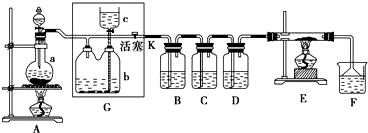
查看答案和解析>>
科目: 来源: 题型:解答题
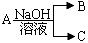 ,(若产物中有水生成则省略未表示出来).
,(若产物中有水生成则省略未表示出来).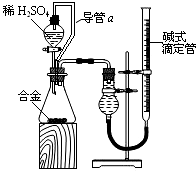
查看答案和解析>>
科目: 来源: 题型:解答题
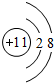 ;YW2的电子式
;YW2的电子式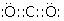 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1种 | B. | 5种 | C. | 6种 | D. | 1000种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、+4、-2 | -2 |
| A. | 沸点:H2T>H2R | |
| B. | 热稳定性:H2T<H2R | |
| C. | 与稀盐酸反应的剧烈程度:L单质<Q单质 | |
| D. | L2+与R2-的核外电子数相等 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 操作及现象 | 结论 | |
| A | 将铜粉加入1.0mol•L-1Fe2(SO4)3溶液中,溶液变蓝 | 金属铁比铜活泼 |
| B | 向某溶液中滴加氯水后再加入KSCN溶液,溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色. | Br-还原性强于Cl- |
| D | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结. | NH4Cl固体可以升华 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com