
科目: 来源: 题型:推断题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分别蘸有浓氨水和浓盐酸的两根玻璃棒靠近时有白烟生成 | |
| B. | 氨气极易溶解于水,因此可用来做喷泉实验 | |
| C. | 氯化铵受热分解有氨气生成,因此实验室可以用加热氯化铵的方法制备氨气 | |
| D. | 氨具有还原性,可以被氧化成NO |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 对燃煤进行脱硫 | |
| B. | 对含SO2、NO2等工业废气进行无害处理后,再排放到大气中 | |
| C. | 人工收集雷电作用所产生的氮的氧化物 | |
| D. | 飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等 |
查看答案和解析>>
科目: 来源: 题型:解答题
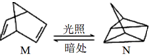 △H=+88.6kJ/mol
△H=+88.6kJ/mol查看答案和解析>>
科目: 来源: 题型:选择题
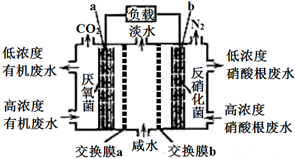
| A. | 电池工作时,电子由a极经导线流向b极 | |
| B. | 交换膜a是阴离子交换膜 | |
| C. | 电极b的反应式:2NO3-+10e-+6H2O=N2↑+12OH- | |
| D. | 相同时间内(相同状况下)生成CO2和N2的体积比为5:2 |
查看答案和解析>>
科目: 来源: 题型:实验题
| 紫铜 | 青铜 | 铜绿 | |
| 主要成分 | 纯铜 | 铜锡合金 | Cu2(OH)2CO3 |
| 性质与用途 | 紫红色,质软,导电性能良好;主要用作电线电缆. | 多呈灰绿色,熔点低、硬度大、可塑性强;可铸造成各种器具. | 不溶于水的灰绿色粉末,溶于酸,加热易分解;可作颜料、杀虫剂. |

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
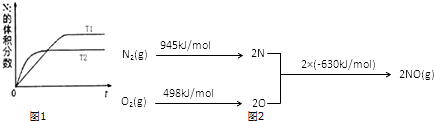
查看答案和解析>>
科目: 来源: 题型:解答题
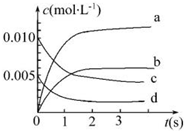 在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器内,800℃时反应2NO(g)+O2(g)=2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用“地沟油”中油脂生产航空生物煤油 | |
| B. | 用细菌浸取法以含硫化铜贫矿制取铜盐 | |
| C. | 用水代替化工合成反应中某些有机 | |
| D. | 将废铅蓄电池深埋处理,节约回收成本 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com