
科目: 来源: 题型:选择题
| A. | H2O>H2Te>H2Se>H2S | B. | HF>HI>HBr>HCl | ||
| C. | SbH3>NH3>AsH3>PH3 | D. | H2O>NH3>HF>CH4 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用洁净的铂丝蘸取溶液在火焰上灼烧,产生黄色火焰,则原溶液中一定不含有K+ | |
| B. | 加入碳酸钠溶液产生白色沉淀,再加入盐酸白色沉淀消失,一定有Ba2+ | |
| C. | 检验Na2CO3固体中是否混有NaHCO3,可向固体滴加稀盐酸,观察是否产生气体 | |
| D. | 向无色溶液中加入稀盐酸无现象,再加入BaCl2有白色沉淀生成,则该溶液中一定含有SO42- |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
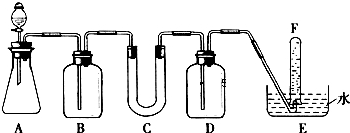
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| C | 石棉绒与过氧化钠 | 与CO2反应,产生O2 |
| D | 吸收未反应的CO2气体 |
查看答案和解析>>
科目: 来源: 题型:解答题
 某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.
某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 糖类、油脂、蛋白质、乙酸都能发生水解反应 | |
| B. | 糖类、油脂、蛋白质都是只由C、H、0三种元素组成的 | |
| C. | 糖类、油脂、蛋白质都是天然高分子化合物 | |
| D. | 油脂有油和脂肪之分,但都属于酯 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 能发生脂化反应的酸一定是羧酸 | |
| B. | 蛋白质溶液中加入浓Na2SO4溶液,蛋白质从溶液中凝聚而析出叫盐析 | |
| C. | 天然蛋白质一定条件下水解的最终产物是α-氨基酸 | |
| D. | 淀粉、纤维素和油脂在一定条件下都能发生水解反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下,1L0.1mol/L的Na2CO3溶液中含有CO32-和HCO3-离子数之和为0.1NA | |
| B. | 标准状况下,11.2L丙烷中含有的极性共价键数目为4NA | |
| C. | 向Fel2溶液中通入适量Cl2,当有1molFe2+被氧化时,共转移的电子数目为NA | |
| D. | 标准状况下,22.4LCl2与足量NaOH溶液反应,转移的电子数为2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 含有羟基的化合物一定属于醇类化合物 | |
| B. | 醇类化合物的官能团是跟链烃基相连的 | |
| C. | 96%的乙醇跟过量的Na混合,加热蒸馏可制得无水乙醇 | |
| D. | 白酒瓶标鉴上的“28°”是指含水28%(体积分数) |
查看答案和解析>>
科目: 来源: 题型:选择题
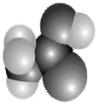 某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示.请根据其结构特点判断下列有关说法中正确的是( )
某常见有机物(只含碳、氢、氧三种元素)分子的比例模型如图所示.请根据其结构特点判断下列有关说法中正确的是( )| A. | 全部正确 | B. | 只有②错误 | C. | 只有③ | D. | 全部错误 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com