
科目: 来源: 题型:选择题
| A. | X的氢化物的沸点可能高于Y的氢化物的沸点 | |
| B. | 原子半径比较:X<Y<Z<W | |
| C. | X2H4与H2W都能使溴水褪色,且褪色原理相同 | |
| D. | 短周期所有元素中,Z的最高价氧化物的水化物碱性最强 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 探究“硫代硫酸钠与酸反应速率的影响因素”的实验中,通过观察产生气体的快慢,来反映试剂反应速率的大小.从而探究浓度温度等外界条件对该反应的化学反应速率的影响 | |
| B. | 容量瓶、滴定管上都标有使用温度和“0”刻度;使用前水洗后滴定管还需润洗,而容量瓶不需要润洗 | |
| C. | 油脂皂化反应后的反应液中加入饱和食盐水并搅拌后出现分层,则生成的高级脂肪酸钠在下层 | |
| D. | 只用 NaHCO3 溶液就可鉴别出稀盐酸、NaOH溶液、AlCl3溶液、NaAlO2 溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硝化甘油在体内能够分解出NO,少量的NO会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛 | |
| B. | 侯氏制碱法的工艺流程应用了物质溶解度的差异 | |
| C. | 刚玉、红宝石、蓝宝石的主要成分是氧化铝,而青花瓷、石英玻璃、分子筛的主要成分是硅酸盐 | |
| D. | 生物炼铜法就是利用某种能耐受铜盐毒性的细菌,利用空气中的氧气把不溶性的硫化铜转化为可溶性的铜盐,从而使铜的冶炼变得成本低,污染小,反应条件十分简单 |
查看答案和解析>>
科目: 来源: 题型:实验题
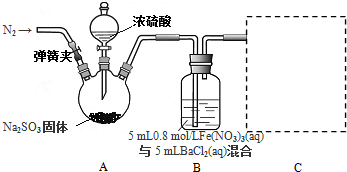
查看答案和解析>>
科目: 来源: 题型:推断题
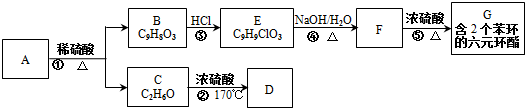
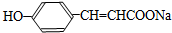 .
.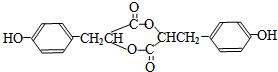 .
.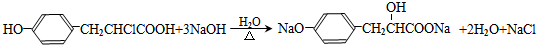 :反应①:
:反应①: .
.查看答案和解析>>
科目: 来源: 题型:推断题
| Y | ||||
| Q | W | X | Z |
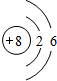 ;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.
;举一例说明Z的非金属性比X的非金属性强的事实:酸性强弱;HClO4>H3PO4,或稳定性:HCl>PH3.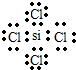 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用饱和食盐水替代水与电石反应,可以减缓乙炔的产生速率 | |
| B. | 配制一定物质的量浓度的溶液定容时,俯视刻度线会使浓度偏低 | |
| C. | 测定中和反应的反应热时,将碱缓慢倒入酸中,不影响测定结果 | |
| D. | 用NaOH标准液滴定待测浓度盐酸,达终点时滴定管尖嘴有悬滴,则测定结果偏小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 食盐可做调味剂、防腐剂 | |
| B. | 硅酸钠可做木材防火剂的原料 | |
| C. | 二氧化硫在葡萄酒中起漂白作用 | |
| D. | 还原铁粉可用于食品包装袋内的脱氧剂 |
查看答案和解析>>
科目: 来源: 题型:推断题
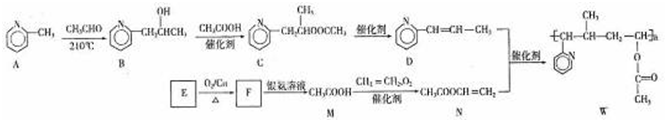
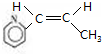 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$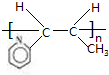 .
. .
.查看答案和解析>>
科目: 来源: 题型:选择题
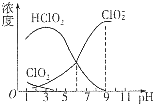 亚氯酸钠(NaClO2)是一种高效漂白剂.在NaClO2溶液中存在ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列说法错误的是( )
亚氯酸钠(NaClO2)是一种高效漂白剂.在NaClO2溶液中存在ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列说法错误的是( )| A. | 亚氯酸钠溶液在碱性条件下较稳定 | |
| B. | 25℃时,HClO2的电离平衡常数的数值Ka=10-6 | |
| C. | 使用该漂白剂的最佳pH约为4 | |
| D. | 25℃时,同浓度的HClO2溶液和NaClO2溶液等体积混合(pH=5.1),则混合溶液中有c(HClO2)+c(H+)=c(ClO${\;}_{2}^{-}$)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com