
科目: 来源: 题型:解答题
 CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.查看答案和解析>>
科目: 来源: 题型:解答题
 甲醇、乙醇、氨气等都是重要的化工原料.
甲醇、乙醇、氨气等都是重要的化工原料.查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 升高温度,该反应的平衡常数将增大 | |
| B. | 从平衡混合气中分离出水蒸气可提高CO2和H2的利用率 | |
| C. | 再向该容器中充入2 mol H2和1 mol CO2,达到平衡时,H2的转化率将小于CO2 | |
| D. | T℃,在起始体积为V L的密闭容器(容积可变,恒压)中将3 mol H2和1 mol CO2混合,达到平衡时乙醇体积分数大于a |
查看答案和解析>>
科目: 来源: 题型:解答题
| A | B |
| ①能使溴的四氯化碳溶液褪色 ②分子比例模型为 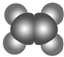 ③能与水在一定条件下反应 | ①由C、H两种元素组成 ②分子球棍模型为  |
查看答案和解析>>
科目: 来源: 题型:解答题
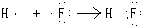 .
. ,写出A、B两元素按1:1原子个数比形成化合物的电子式
,写出A、B两元素按1:1原子个数比形成化合物的电子式 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:推断题

 ,化合物J的俗名纯碱.
,化合物J的俗名纯碱.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 22.4LO3中含3NA个氧原子 | |
| B. | 标准状况下,22.4LCH2Cl2含有2NA氯原子 | |
| C. | 1molSO2与足量的H2S充分反应,转移NA个电子 | |
| D. | 16gCH4中含有10NA个质子 |
查看答案和解析>>
科目: 来源: 题型:解答题
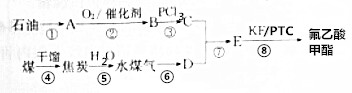
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com