
科目: 来源: 题型:选择题
| A. | 全部 | B. | ①②③④⑥ | C. | 只有①②③ | D. | 只有②③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 蛋白质在紫外线的照射下会失去生理活性 | |
| B. | 蛋白质溶液不能产生丁达尔效应 | |
| C. | 蛋白质溶液中加入CuSO4可产生盐析现象 | |
| D. | 蚕丝、羊毛、棉花的主要成分都是蛋白质 |
查看答案和解析>>
科目: 来源: 题型:解答题
 A、B、C三种固体物质的溶解度曲线如图所示.
A、B、C三种固体物质的溶解度曲线如图所示.查看答案和解析>>
科目: 来源: 题型:选择题
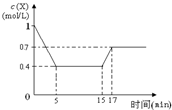 一定条件下,向密闭容器中加入1mol/L X发生反应:3X(g)?Y(g)+Z(g)△H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是( )
一定条件下,向密闭容器中加入1mol/L X发生反应:3X(g)?Y(g)+Z(g)△H<0,反应到5min时达到平衡,在15min时改变某一条件,到17min时又建立新平衡,X的物质的量浓度变化如图,下列说法中不正确的是( )| A. | 0~5 min时,该反应的速率为v(X)=0.12 mol/(L•min) | |
| B. | 15 min时改变的条件可能是减小压强 | |
| C. | 15 min时改变的条件可能是升高温度 | |
| D. | 从初始到17 min时,X的转化率为30% |
查看答案和解析>>
科目: 来源: 题型:解答题
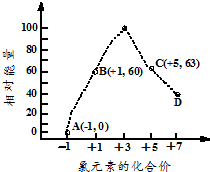 填写下列空白:
填写下列空白: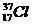 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
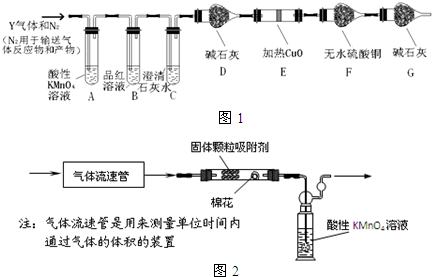
查看答案和解析>>
科目: 来源: 题型:解答题
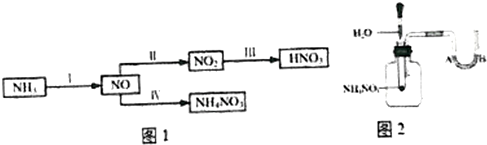
查看答案和解析>>
科目: 来源: 题型:解答题
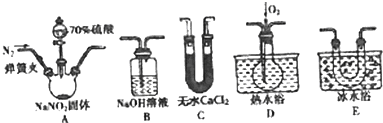
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com