
科目: 来源: 题型:多选题

| A. | 燃料电池的正极反应式为:O2+2H2O+4e-=4OH- | |
| B. | 装置中NaOH溶液的作用是吸收产生的有毒气体氯气 | |
| C. | 装置中的电子流动路径为:负极→外电路→阴极→苦卤水→阳极→正极 | |
| D. | 理论上,当b 极周围产生2g H2,电池消耗C6H12O6的质量为15g |
查看答案和解析>>
科目: 来源: 题型:解答题
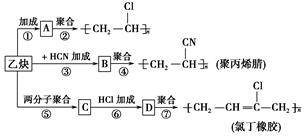

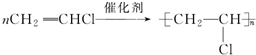 ;
;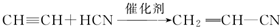 ;
;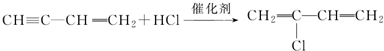 .
.查看答案和解析>>
科目: 来源: 题型:解答题
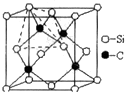 碳、氮、氟、硅、钛等元素的化合物广泛应用于生产生活,回答下列问题:
碳、氮、氟、硅、钛等元素的化合物广泛应用于生产生活,回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 其水溶液导电的一定是离子晶体 | |
| B. | 固态导电的一定是金属晶体 | |
| C. | 共价化合物形成的晶体一定是分子晶体 | |
| D. | 固态不导电、熔融态导电的一定是离子晶体 |
查看答案和解析>>
科目: 来源: 题型:填空题
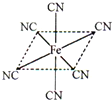 铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图;已知CN-与N2结构相似,1molCN-中π键数目为2NA.
铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图;已知CN-与N2结构相似,1molCN-中π键数目为2NA.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com