
科目: 来源: 题型:选择题
| A. | CO、NO均难溶于水 | |
| B. | CO、NO均为酸性氧化物 | |
| C. | CO、NO均为无色无味的有毒气体 | |
| D. | 在催化剂的作用下,可通过反应2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2来达到净化汽车尾气的目的 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1 mol CH≡CH可以与Br2发生加成反应,消耗2 mol Br2 | |
| B. | 苯的邻位二元取代物只有一种可以说明苯分子不具有碳碳单键和碳碳双键的交替结构 | |
| C. | 2甲基戊烷的沸点高于己烷 | |
| D. | 用水可区分苯和溴苯 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 计算机芯片的组成元素位于第14纵行 | |
| B. | 第10纵行元素全部是金属元素 | |
| C. | 第3纵行元素的种类最多 | |
| D. | 只有第2纵行元素的原子最外层有2个电子 |
查看答案和解析>>
科目: 来源: 题型:解答题
 有机物M的结构简式如图所示.
有机物M的结构简式如图所示.查看答案和解析>>
科目: 来源: 题型:解答题
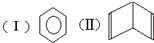 人们对苯及芳香烃的认识有一个不断深化的过程.
人们对苯及芳香烃的认识有一个不断深化的过程.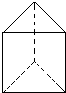 :该结构的一氯代物有1种.
:该结构的一氯代物有1种. ,下列关于萘的说法正确的是CD(填编号)
,下列关于萘的说法正确的是CD(填编号)查看答案和解析>>
科目: 来源: 题型:解答题
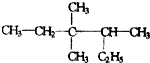 3,3,4-三甲基己烷
3,3,4-三甲基己烷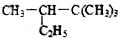 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷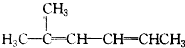 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯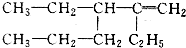 2,3-二乙基-1-己烯.
2,3-二乙基-1-己烯.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
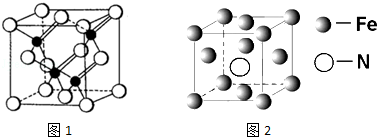
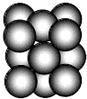 现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题
现有六种元素,其中B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F 是前四周期原子电子轨道表示式中单电子数最多的元素 |
| G在周期表的第十一列 |
 →
→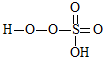 +HE (请写出横线上物质的结构式)
+HE (请写出横线上物质的结构式)查看答案和解析>>
科目: 来源: 题型:解答题
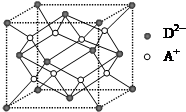 有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B- 少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A+ 与D2- 离子数之比为2:1.请回答下列问题:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B- 少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数.R是由A、D两元素形成的离子化合物,其中A+ 与D2- 离子数之比为2:1.请回答下列问题: ,在CB3 分子中C元素原子的原子轨道发生的是sp3 杂化.
,在CB3 分子中C元素原子的原子轨道发生的是sp3 杂化.查看答案和解析>>
科目: 来源: 题型:多选题
| A. | CCl4和SiCl4的熔点 | B. | NH3与H2O的键角 | ||
| C. | SO2和CO2在水中的溶解度 | D. | 碳化硅和金刚石的硬度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com