
科目: 来源: 题型:选择题
| A. | 核内的中子数为53 | |
| B. | 核内的电子数为135 | |
| C. | 核内的中子数与核外电子数之差为29 | |
| D. | 质量数为82 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液和溴水因发生化学反应而褪色 | |
| B. | 不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗 | |
| C. | 配制银氨时,应将大量浓氨水一次性加入到少量硝酸银溶液中 | |
| D. | 用银氨溶液或新制氢氧化铜来检验醛或酮时,均只需要水浴加热 | |
| E. | 配制氢氧化铜悬浊液时,应将少量硫酸铜溶液加入到过量的氢氧化钠溶液中 |
查看答案和解析>>
科目: 来源: 题型:解答题
操作 | 现象 |
| 向盛有4g CaO2的大试管中加入10mL稀盐酸的溶液a | 剧烈反应,产生能使带火星木条复燃的气体 |
| 取5mL溶液a于试管中,滴入两滴石蕊 | 溶液变红,一段时间后溶液颜色明显变浅,稍后,溶液变为无色 |

查看答案和解析>>
科目: 来源: 题型:解答题
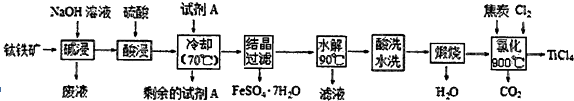
查看答案和解析>>
科目: 来源: 题型:解答题
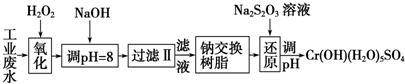
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | KMnO4 | B. | NaClO | C. | Ca(ClO)2 | D. | HNO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
 A是在人们日常生活中最常见的有机物,75%(体积分数)的水溶液可用于医疗消毒,B是一种植物生长调节剂,通常情况下C是一种具有果香味的无色液体.
A是在人们日常生活中最常见的有机物,75%(体积分数)的水溶液可用于医疗消毒,B是一种植物生长调节剂,通常情况下C是一种具有果香味的无色液体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com