
科目: 来源: 题型:解答题
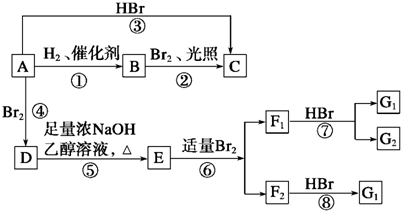
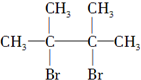 .
.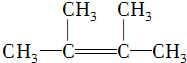 ,其名称为2,3-二甲基-2-丁烯.
,其名称为2,3-二甲基-2-丁烯. .
.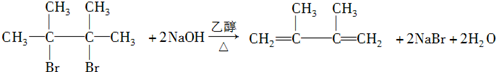 ;写出由E→F2的化学方程式
;写出由E→F2的化学方程式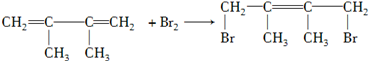 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c(Fe3+)=0.1mol•L -1的溶液中:K+、NH4+、CO32-、SO42-能共存 | |
| B. | 与Al反应产生H2的溶液中,NO3-、Na+、SO42-、Fe2+一定不共存 | |
| C. | NaClO溶液中通入少量SO2:2ClO-+SO2+H2O═SO32-+2HClO | |
| D. | 用铜作电极电解NaCl溶液:2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- |
查看答案和解析>>
科目: 来源: 题型:选择题
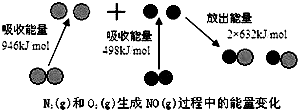
| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 通常情况下,N2(g)和O2(g)混合能直接生成NO | |
| C. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 每一周期元素都是从碱金属开始,以稀有气体结束 | |
| B. | f区都是副族元素,s区和p区的都是主族元素 | |
| C. | 铝的第一电离能小于K的第一电离能 | |
| D. | B电负性和Si相近 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2CO3 | B. | Na2O2 Na2CO3 | ||
| C. | NaOH Na2CO3 | D. | Na2O2 NaOH Na2CO3 |
查看答案和解析>>
科目: 来源: 题型:解答题
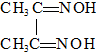 )作用生成腥红色配合物沉淀A.
)作用生成腥红色配合物沉淀A.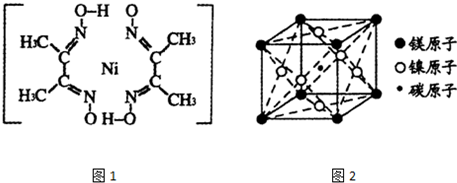
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCO3-,Cl-,Na+,NH4+ | B. | AlO2-,S2-,Na+,K+ | ||
| C. | SiO32-,CO32-,K+,Na+ | D. | Ba2+,Al3+,NO3-,Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com