
科目: 来源: 题型:选择题
| A. | $\frac{Kw}{c({H}^{+})}$=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- | |
| B. | 加入铝粉生成H2的溶液:K+、Mg2+、SO42-、HCO3- | |
| C. | c(Fe3+)=0.1 mol/L的溶液:Fe2+、Al3+、Cl-,CO32- | |
| D. | 能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 二氧化硅为酸性氧化物,可用于制做计算机芯片 | |
| B. | 铜的金属活泼性比铁差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| C. | Zn具有还原性和导电性,可用作锌锰干电池的负极材料 | |
| D. | 浓硫酸具有脱水性,可用于干燥NH3、SO2等 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲烷分子的球棍模型: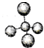 | B. | NH4Br的电子式: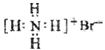 | ||
| C. | 氯原子的结构示意图: | D. | 邻羟基苯甲酸的结构简式: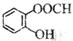 |
查看答案和解析>>
科目: 来源: 题型:选择题
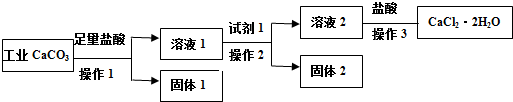
| A. | 试剂1可以是适量的氢氧化钙固体或适量的氧化钙固体 | |
| B. | 欲检验溶液2中是否含有Fe3+,可取少量溶液,滴加KSCN溶液,若溶液无明显现象,则不含有Fe3+ | |
| C. | 若用已知浓度AgNO3溶液来滴定产品(加入某指示剂)中的氯离子来测量产品纯度,计算所得的数据不可能大于100.0% | |
| D. | 若改变方案,在溶液2中加入适量的碳酸铵,得到的沉淀用盐酸溶解、酸化后进行操作3,可得到纯度更高的二水合氯化钙 |
查看答案和解析>>
科目: 来源: 题型:选择题
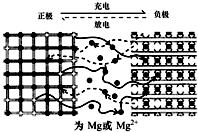 镁离子电池以金属镁或镁合金为负极,以能嵌入镁离子的化合物为正极,其工作原理如图所示,反应原理为:xMg+Mo3S4$?_{充电}^{放电}$ MgxMo3S4,下列说法不正确的是( )
镁离子电池以金属镁或镁合金为负极,以能嵌入镁离子的化合物为正极,其工作原理如图所示,反应原理为:xMg+Mo3S4$?_{充电}^{放电}$ MgxMo3S4,下列说法不正确的是( )| A. | 放电时,电池中的Mg2+从负极移向正极 | |
| B. | 其负极反应为:xMg-2xe-+Mo3S42x-═MgxMo3S4 | |
| C. | 充电时阳极反应式:MgxMo3S4-2xe-═Mo3S4+xMg2+ | |
| D. | 由于镁的密度较小,且Mg2+携带两个正电荷,这为高能量电池的设计提供了一个可靠依据 |
查看答案和解析>>
科目: 来源: 题型:实验题
| 装置 | 序号 | 试管中的药品 | 现象 |
持续通入 | 实验Ⅰ | 1.5mL 1mol•L-1 CuSO4溶液和3.5mL 1mol•L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5mL 1mol•L-1 CuCl2溶液和3.5mL 1mol•L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
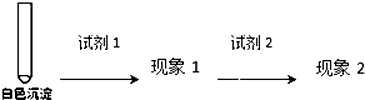
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:推断题
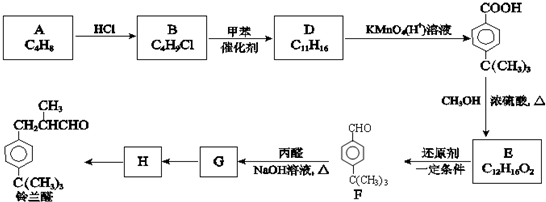
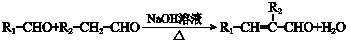
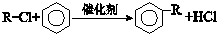
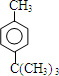 .
.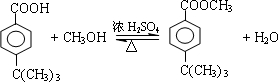 .
.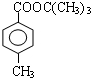 、
、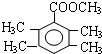 .(写出两种即可)
.(写出两种即可)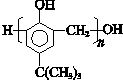 ,合成路线是
,合成路线是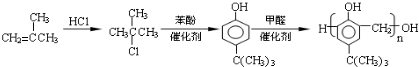 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 青砖(含Fe3O4)中的Fe2+可用浓盐酸溶解后,再加入适量高锰酸钾溶液进行检验 | |
| B. | 用0.1000 mol•L-1 NaOH溶液滴定20.00 mL未知浓度盐酸,接近终点时因滴速太快造成NaOH少许过量;此时若加入一定体积该盐酸后,继续用该NaOH溶液恰好滴定至终点,则测得的盐酸浓度将偏大 | |
| C. | 用镊子夹取金属钠固体,切割取用后剩余的钠放回原试剂瓶中 | |
| D. | 检查容量瓶瓶口是否漏水的方法是:往瓶内加入一定量水,塞好瓶塞.用食指摁住瓶塞,另一只手托住瓶底,把瓶倒转过来,观察瓶塞周围是否有水漏出即可 |
查看答案和解析>>
科目: 来源: 题型:实验题
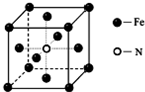 NH3在工农业生产中具有重要的作用,可以用来生产尿素等化学肥料,也可以用来制备一些配位化合物.
NH3在工农业生产中具有重要的作用,可以用来生产尿素等化学肥料,也可以用来制备一些配位化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com