
科目: 来源: 题型:选择题
| A. | Na2O2可用作呼吸面具中的供氧剂 | |
| B. | 氨气可做制冷剂 | |
| C. | Al(OH)3可作治疗胃酸过多的一种药剂 | |
| D. | 包装食品里常有硅胶、生石灰、还原铁粉等,其作用相同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甲苯的一氯代物 | B. | 分子式为C5H10的烯烃 | ||
| C. | 相对分子质量为74的一元醇 | D. | 立方烷( )的二硝基取代物 )的二硝基取代物 |
查看答案和解析>>
科目: 来源: 题型:解答题

 、
、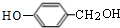 .
. .
. .
.查看答案和解析>>
科目: 来源: 题型:填空题
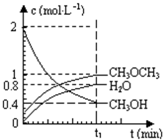 已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题:
已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 消耗B 0.08mol | B. | x=2 | ||
| C. | A的平衡浓度是1.4mol/L | D. | 平衡时气体压强是原来的0.94倍 |
查看答案和解析>>
科目: 来源: 题型:填空题
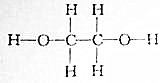
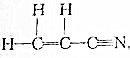
查看答案和解析>>
科目: 来源: 题型:实验题
 如图是实验室制取并探究氯气化学性质的装置图
如图是实验室制取并探究氯气化学性质的装置图查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com