
科目: 来源: 题型:实验题
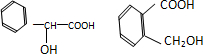 等(写一种即可)
等(写一种即可)查看答案和解析>>
科目: 来源: 题型:填空题
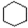 $→_{①}^{Cl_{2}光照}$
$→_{①}^{Cl_{2}光照}$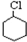 $→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2}不见光}$B$\stackrel{④}{→}$
$→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2}不见光}$B$\stackrel{④}{→}$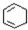 $\stackrel{⑤}{→}$
$\stackrel{⑤}{→}$ $\stackrel{⑥}{→}$C$→_{⑦}^{H_{2}}$
$\stackrel{⑥}{→}$C$→_{⑦}^{H_{2}}$
 ,C
,C .
.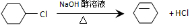 反应⑤
反应⑤ .
.查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:实验题
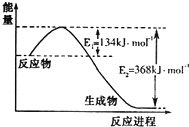 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答:
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答:| t/K | 298 | 398 | 498 | … |
| K/(mol•L-1) | 4.1×106 | K1 | K2 | … |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2c(H+)═2c(HS-)+c(S2-)+2c(OH-)? | B. | c(H+)═c(HS-)+2c(S2-)+c(OH-) | ||
| C. | c(H+)═c(HS-)+2c(S2-)? | D. | c(H+)═2c(S2-)+c(OH-)? |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 30 L | B. | 20 L | C. | 10 L | D. | 40 L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定大于92.0 kJ | B. | 一定等于92.0 kJ | C. | 一定小于92.0 kJ | D. | 不能确定 |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:计算题
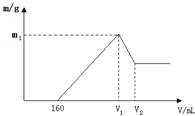 将镁铝的混合物0.1mol溶于100mL2mol/L硫酸溶液中,然后再滴加1mol/L氢氧化钠溶液,请回答以下问题:
将镁铝的混合物0.1mol溶于100mL2mol/L硫酸溶液中,然后再滴加1mol/L氢氧化钠溶液,请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com