
科目: 来源: 题型:填空题
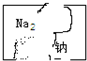 实验室发现一瓶标签破损的溶液,如图所示,同学猜想,该溶液可能是C.(填字母序号)
实验室发现一瓶标签破损的溶液,如图所示,同学猜想,该溶液可能是C.(填字母序号)查看答案和解析>>
科目: 来源: 题型:选择题
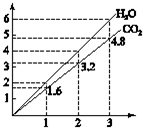 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )| A. | ②⑤⑥ | B. | ④⑥ | C. | ①②④ | D. | ②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④ | B. | ②⑤⑥ | C. | ②③⑤ | D. | ①④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.5mol | B. | 2mol | C. | 2.5mol | D. | 4mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径 Cl>Si>Na | B. | 金属性 Na>Mg>Al | ||
| C. | 碱性 LiOH>NaOH>KOH | D. | 酸性 H3PO4>H2SO4>HClO4 |
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:推断题
| 物质 | 分子的价层电子对数 | 中心原子的杂化轨道类型 | 分子的立体构型名称 |
| X2Z | V形 | ||
| YZ2 |
查看答案和解析>>
科目: 来源: 题型:填空题
| 第一电离能 | 电负性 | 氢化物沸点 | 最高价氧化物对应水化物的碱性 |
| W<X | Z>Y | Y<Z | W>X |
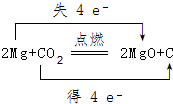 .
.查看答案和解析>>
科目: 来源: 题型:填空题
| 元素 | 元素性质或原子的结构 |
| T | 2p轨道能级电子数比s能级电子数多1个 |
| X | L层p能级电子数比s能级电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有3个未成对电子 |
 .写出元素Z的简单气态氢化物的电子式:
.写出元素Z的简单气态氢化物的电子式: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com